蒙脱石(MMT)是一种水敏性很强的层状硅酸盐矿物,水分子极易进入层间致使体积急剧增大。泥页岩中蒙脱石的水化膨胀引起岩石力学性质下降,对油田钻探、巷道以及路基施工造成很大的危害[1-3]。在煤炭洗选过程中,蒙脱石含量高的矸石极易泥化产生高灰细泥,严重影响分选和煤泥水沉降效果。
为抑制蒙脱石的水化膨胀,油田生产中开发了大量的黏土稳定剂。在煤泥水处理领域,杨林青[4]和王冉[5]等也相继展开了无机盐、有机小阳离子TMBAC抑制蒙脱石的水化膨胀以及对煤泥浮选和压滤脱水影响的研究。季铵盐小阳离子是一种近年来用于抑制黏土水化膨胀的高效的有机小阳离子,是国内外最具发展前景的一类黏土稳定剂[6]。有学者[7-8]采用X射线衍射分析、Zeta电位分析和相对润湿接触角测试等方法对小阳离子稳定剂的抑制机理进行了研究。结果表明小阳离子稳定剂可交换出黏土层间的水化阳离子并吸附在层间,强静电作用使其脱附比较困难。同时,小阳离子在黏土表面吸附后阻碍了水分子与表面的接触,但并不会改变颗粒表面的亲水性。2-羟乙基三甲基氯化铵是油田生产中常用的小阳离子黏土稳定剂,俗称氯化胆碱[9](LHDJ),分子式为C5H14ClNO,其防膨率高、稳定、长效,且安全环保,可作为煤泥水处理中蒙脱石水化膨胀的抑制剂。
研究稳定剂的微观作用机理对设计和选择高效合理且适用于煤泥水处理的药剂有重要的意义。实验研究可以体现药剂与蒙脱石之间宏观的作用效果,但很难在分子水平上观察它们之间微观反应过程和作用机理。量子化学方法(DFT)广泛应用于研究吸附质在矿物表面吸附时的原子和电子性质,可以从分子水平上理解黏土稳定剂的作用机理。陈建华等[10]应用密度泛函理论研究了羟基钙在黄铁矿表面的吸附行为。郗朋等[11]研究了黄铁矿表面碳质掺杂和吸附。陈军[12]、韩永华[13]等分别研究了铵/铵阳离子、羟基钙在高岭石表面的吸附机理。SHI等[14]研究了NH4+离子在蒙脱石层间的吸附机理以及离子在层间的水化行为。
黏土稳定剂的作用机理目前主要集中在实验研究,分子水平上的模拟研究较少。本文利用Materials Studio软件中的Adsorption Locator模块构建了药剂在蒙脱石表面吸附的较优构型,通过吸附能的计算确定最优构型,并利用密度泛函理论的平面波贋势方法计算了最优构型的成键情况、态密度和电荷变化,以探究LHDJ抑制蒙脱石水化的作用机理。
1 计算方法和模型
1.1 蒙脱石晶胞结构优化参数的选取
蒙脱石是典型的2∶1型层状黏土矿物,两层硅氧四面体夹着一层铝氧八面体。本文参考VOORA[15]所述方法构建了蒙脱石晶体模型,晶体中1个Mg2+取代1个Al3+。四面体片表面每6个氧原子和6个硅原子形成1个环状结构,其中6个氧原子形成了氧六元(SOR)环结构,Na+被置于相邻两晶层氧六元环中央。晶胞结构式为NaSi8Al3MgO20(OH)4,计算中使用2×1×1的超晶胞模型,共包含两个晶胞。蒙脱石原始晶胞的优化采用Materials Studio软件的Castep模块,选取对氢键描述比较精确的GGA-PBE[16]交换关联函数。同时由于蒙脱石相邻两个层面间通过范德华力联结,因此选择DFT-D方法对色散力修正[17],平面波截断能经过收敛测试后取405 eV。优化算法采用BFGS算法,自洽场SCF收敛精度设为2.0×10-6 eV/atom[13,18]。几何优化的收敛标准:原子最大位移0.000 2 nm,原子间作用力0.05 eV/10-10 m,原子间内应力0.1 GPa,体系总能量变化2.0×10-5 eV/atom。所有计算均在倒易空间中进行,计算中所涉及原子的赝势计算选取旳价电子分别为Si 3s23p2,Mg 2s22p63s2,Al 3s23p,O 2s22p4,H 1s,Na 2s22p63s,Cl 3s23p5。
蒙脱石的层间距是其一个重要参数,建模方法及模型中Mg/Al置换比都会影响晶胞的层间距。本文优化后蒙脱石层间距为9.587×10-10 m,与文献[15]实验测得的Na-蒙脱石层间距9.600×10-10 m相当接近,这表明本文构建的模型及采用的计算参数合理。在表面模型及吸附构型的DFT计算中,均采用与体相晶胞模型优化一致的计算参数。
1.2 计算方法
图1(a)为Na-蒙脱石的晶体结构(紫色、白色、红色、黄色、绿色、粉色和绿色分别代表Na,H,O,Si,Al 和Mg),可知当晶体沿001晶面解离时,同时形成含Na离子的Na-001面以及不含Na离子的None-001面,两类表面所含Na离子不同,所以性质也有很大的差别。因此,蒙脱石001表面模型由体相晶胞模型沿(001)面切出,并在表面添加20×10-10 m的真空层得到含Na离子的Na-001以及不含Na离子的None-001表面模型。图1(b)显示了蒙脱石的层状结构,小阳离子LHDJ会与层间的补偿阳离子(Na+)发生交换,从而吸附在蒙脱石的层间。表面模型沿c轴方向含有一层晶胞结构,共包含“O-Si-O-Al(Mg)-O-Si-O-Na”,考虑到Mg/Al原子置换的影响,在表面优化时,仅固定底部3层原子,对上部的Al(Mg)-O-Si-O-(Na)层进行表面弛豫;层间模型与表面模型使用同样的方法弛豫。

图1 Na-蒙脱石的晶体结构
Fig.1 Unit cell of Na-MMT
为确定单个药剂分子在蒙脱石表面的初始吸附构型,对DFT优化后药剂和表面模型分配Mulliken电荷,采用基于蒙特卡洛(Monte Carlo,简称MC)方法的Adsorption Locator模块构建药剂在蒙脱石表面吸附的初始构型,然后对吸附能较低的几个构型进行更进一步的DFT优化,最后根据吸附能选择最优的构型。MC计算的条件是:采用UFF力场,每次循环进行105步,共设置10次循环;范德华力的计算采用Atom Based求和法,静电作用的计算采用Ewald & Group求和法。
1.3 吸附能计算
当吸附质在蒙脱石表面发生吸附时体系会释放能量,其吸附能表达式为
Eads=Ead/MMT-(Ead+EMMT)
(1)
式中,Eads为吸附能;Ead和EMMT分别为吸附前吸附质和蒙脱石的总能量;Ead/MMT为吸附质在蒙脱石表面吸附后体系总能量。吸附能为负表示能发生吸附,且吸附能绝对值越大,吸附越稳定。
2 结果及讨论
2.1 LHDJ在蒙脱石表面的吸附机理
2.1.1 初始吸附构型
LHDJ在蒙脱石Na-001,None-001表面和晶层间吸附的3种较优构型,如图2~4所示。LHDJ在蒙脱石层间吸附稳定后,层间距稳定在14.49×10-10 m。对初始吸附构型进行DFT优化,并根据吸附能选择最稳定构型进行键的布居值、态密度和差分电荷密度分析。吸附能计算结果见表1。

图2 MMT-LHDJ系统中LHDJ在蒙脱石Na-001面吸附的3种初始吸附构型
Fig.2 Three low-energy configurations of LHDJ adsorption on MMT Na-001 surface in the MMT-LHDJ system

图3 MMT-LHDJ系统中LHDJ在蒙脱石None-001面吸附的3种初始吸附构型
Fig.3 Three low-energy configurations of LHDJ adsorption on MMT None-001 surface in the MMT-LHDJ system

图4 MMT-LHDJ系统中LHDJ在蒙脱石内表面吸附的3种初始吸附构型
Fig.4 Three low-energy configurations of LHDJ adsorption on the MMT internal surfaces in the MMT-LHDJ system
由表1可知,LHDJ在蒙脱石001表面和层间吸附能绝对值都很大,能稳定吸附。LHDJ在蒙脱石Na-001表面吸附的3种较优构型中,羟基氧原子都指向钠离子,这说明钠离子对羟基氧原子间有很强的吸引作用。在None-001表面,铵基部分位于氧六元环上方,便于氢原子和表面氧原子相互作用。在蒙脱石的层间,LHDJ位于上下两表面的中间,同时与两个表面发生吸附。
2.1.2 LHDJ在蒙脱石表面成键分析
表2列出了LHDJ在蒙脱石表面吸附后最优构型中成键原子的Mulliken布局和键长。在M(Na-001)L-1构型中,由于Na离子和O原子间无共价作用,不能采用键布居值的方式分析其作用强弱。但Na离子和O原子间距离为2.248×10-10 m,比两原子的半径之和2.520×10-10 m小0.272×10-10 m,且Na离子与六元环氧原子间的平均距离从2.606×10-10 m增加到2.611×10-10 m,说明两原子间的作用较强,使Na离子远离表面。当H,O原子之间距离在2.14×10-10~2.56×10-10 m时,存在中等或弱的氢键[19]。
表1 MMT-LHDJ和MMT-LHDJ-2H2O系统中的吸附能
Table 1 Adsorption energies in the MMT-LHDJ and MMT-LHDJ-2H2O systems
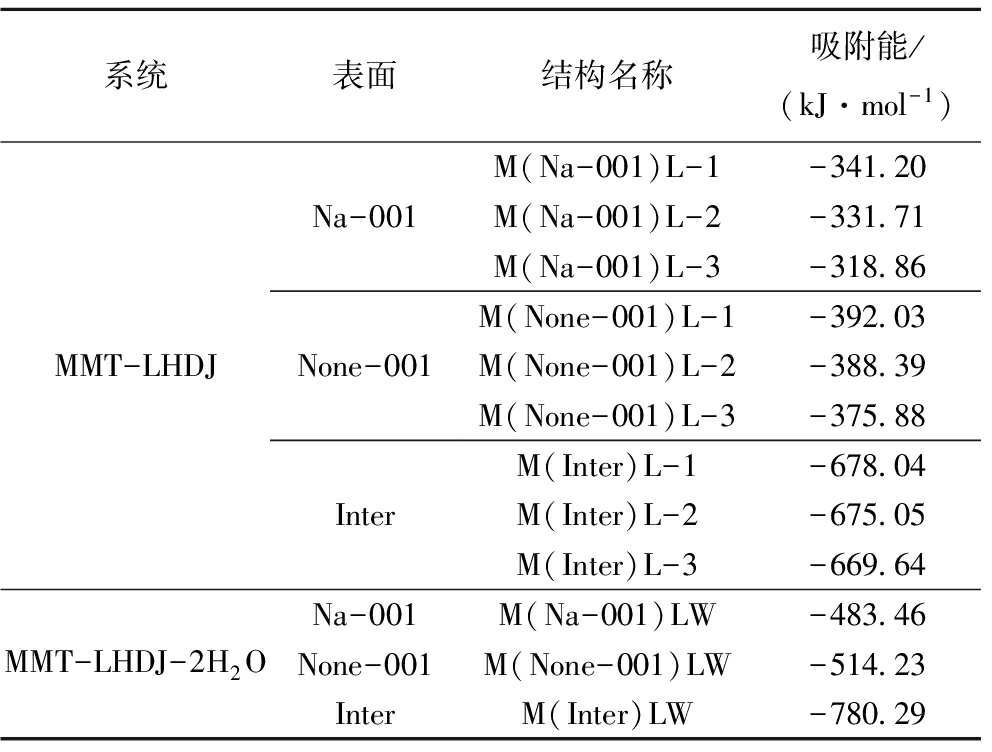
注:表中L代表LHDJ,W代表水分子。
表2 LHDJ在蒙脱石表面吸附后键的Mulliken布局和键长
Table 2 Mulliken population and bond length of LHDJ adsorbed on MMT-001 and internal surfaces

在None-001表面LHDJ与表面六元环氧原子形成了4条氢键,键长分别为2.200×10-10,2.227×10-10,2.283×10-10和2.485×10-10 m,相应的布居值分别为0.02,0.02,0.01和0。虽然每个氢键都较弱,但4个氢键的共同作用也极大地增强了LHDJ在None-001表面的吸附。LHDJ在蒙脱石层间的最稳定构型M(Inter)L-1中仅形成一条较弱的氢键,利于LHDJ在层间的吸附。
2.1.3 LHDJ在蒙脱石表面吸附的态密度分析
根据成键分析,可知LHDJ中O原子和Na-001表面的Na离子存在较强的作用,因此选择这两原子进行吸附前后的态密度分析,结果如图5所示。在整个能级范围内O原子和Na离子态密度局域性都很强,在费米能级以下无明显的原子轨道重叠,表明两原子间无共价键形成。但对比吸附前后两原子的态密度可以发现,作用后O原子态密度整体向低能级移动,远离费米能级,O原子的反应活性降低;Na离子整体也向低能级方向移动,虽然作用后反键轨道在费米能级附近活跃,但其峰值降低,反键作用很弱。Na离子和O原子作用后体系的活性降低,有利于体系稳定。

图5 LHDJ在蒙脱石Na-001面吸附前后原子的态密度
Fig.5 DOS of atom before and after LHDJ adsorption on Na-001 surface
在None-001表面,选取成氢键的4对H,O原子为研究对象,分析其吸附前后的态密度变化以及成键情况。图6为LHDJ在蒙脱石None-001面吸附前后原子的态密度图。可见,H原子的s轨道吸附前费米能级附近态密度较高,说明H原子活性较高,在5~10 eV反键轨道的态密度峰值很强。吸附后,H原子的反键轨道向费米能级移动,集中在0~2 eV,但峰值却大大降低,有利于键的形成;氢原子的s轨道和氧原子的2s,2p轨道都向低能级的方向移动,费米能级附近的态密度减少,降低了体系的能量;在-14~-5 eV氢原子s轨道和氧原子2p轨道重叠,有很强的成键作用。氢原子和氧原子的成键作用有利于体系能量的降低,使LHDJ吸附在None-001表面更牢固。

图6 LHDJ在蒙脱石None-001面吸附前后原子的态密度
Fig.6 DOS of atom before and after LHDJ adsorption on None-001 surface
2.1.4 电荷分析
差分电荷密度定义为成键后的电荷密度与对应点的原子电荷密度之差。通过差分电荷密度的计算和分析,可以清楚地得到在成键和成键电子耦合过程中的电荷移动以及成键极化方向等性质。图7为LHDJ在蒙脱石001表面和层间吸附的差分电荷密度图(黄色区域表示电子密度减小,蓝色区域表示电子密度的增加)。表3列出了LHDJ在蒙脱石001表面和层间吸附前后LHDJ的荷电量变化(LHDJ初始电荷设为0)。

图7 MMT-CHPTA系统中LHDJ在蒙脱石001表面和内表面吸附的差分电荷密度(等值面值为0.007 electrons/10-30 m3)
Fig.7 Electron density difference of LHDJ adsorption on MMT-001 and internal surfaces in the MMT-CHPTA system (Isosurface value is 0.007 electrons/10-30 m3)
由图7中M(Na-001)L-1的差分电荷密度图可知,LHDJ与Na-001表面间的电荷转移在Na,O原子间比较强烈,Na离子周围的电荷密度减小而O原子周围电荷密度增大,电子通过Na-O原子向LHDJ转移。但同时LHDJ中多个H原子向表面O原子转移电荷,所以整体上LHDJ荷0.51 e正电。LHDJ与None-001表面电荷转移量明显强于Na-001,O原子周围电子密度增加,而H原子周围电子密度减小,且形成氢键的H,O原子间电子的积聚强烈,氢键越强,这种电子积聚越强,氢键的形成加剧了电子的转移。LHDJ向None-001表面转移了0.76 e,吸附也更牢固。在晶层间H原子与表面O原子间电荷转移强度较弱,仅在形成氢键的H,O原子间有较强的电子转移,但因层间距较小,药剂其与上下两个面均发生电子转移,转移的电荷量反而最多为0.89 e,吸附能绝对值也最大。
表3 MMT-LHDJ 和MMT-LHDJ-2H2O系统中LHDJ在蒙脱石表面吸附后的荷电量变化
Table 3 Charge changes of LHDJ in the MMT-LHDJ and MMT-LHDJ-2H2O system

对比LHDJ在Na-001,None-001表面的吸附能(-341.20,-392.03 kJ/mol)、电荷转移量(0.51,0.76 e)和氢键数量(0,4个),可以看出Na离子在Na-001表面的存在阻碍了LHDJ与表面间的电子转移以及氢键的形成,不利于LHDJ在001表面的吸附。
2.2 H2O对LHDJ在蒙脱石表面吸附的影响
由于LHDJ在蒙脱石表面的吸附发生在水溶液中,因此研究水分子对LHDJ在蒙脱石表面吸附的影响有很重要的意义。为研究水分子对LHDJ吸附的影响,模拟了两个水分子在蒙脱石表面的吸附,然后利用水分子在表面吸附的最稳定构型来研究水分子的存在对LHDJ吸附的影响,这个方法已用于甲酰胺[20]和羟基钙[21]在蒙脱石表面吸附研究中。图8显示了两个水分子在蒙脱石各表面的最稳定构型。可以看出,水分子易吸附在Na-001表面上的钠离子周围;在None-001表面,第一个水分子与表面形成两个氢键,第二个水分子通过氢键与第一个水分子相连;水分子在层间(层间距设为14.49×1010 m)的吸附与在None-001表面吸附相似。水分子在蒙脱石Na-001表面、None-001表面和层间的吸附能分别为-107.93,-55.30和-61.77 kJ/mol。
将LHDJ和两个水分同时添加到蒙脱石各表面,经MC和DFT优化后,图9展示了水分子存在时LHDJ在蒙脱石各表面吸附的最佳构型。表4列出了MMT-LHDJ-2H2O系统中的成键情况和键的Mulliken布居值。

图8 两个水分子在蒙脱石各表面吸附的最稳定构型
Fig.8 Most stable configurations of the two water molecules adsorbed on MMT

图9 MMT-LHDJ-2H2O系统中LHDJ在蒙脱石表面吸附的最稳定构型
Fig.9 Most stable configurations of LHDJ adsorption on the MMT surfaces in the MMT-CHPTA-2H2O system
表4 MMT-LHDJ-2H2O系统中成键及键的布居值
Table 4 Bond Mulliken population and length of MMT-LHDJ-2H2O system

可以看出,水分子的存在对LHDJ在各表面的吸附产生很大的影响。M(Na-001)LW系统吸附能的绝对值为483.46 kJ/mol,大于其子系统M(Na-001)L-1(-341.20 kJ/mol)和M(Na-001)W(-107.93 kJ/mol)的吸附能绝对值之和449.13 kJ/mol,水分子和LHDJ展现出协同吸附[20-21]。在Na-001表面,两个水分子优先吸附在钠离子周围,LHDJ中氧原子与钠离子间的静电作用力消失。此时,两个水分子与表面钠离子作用的同时与LHDJ中的羟基形成两个氢键,键长分别为1.863×10-10和1.938×10-10 m,对应的布居值分别为0.08和0.06,两个水分子将LHDJ与表面桥联起来。吸附稳定后,LHDJ的正电位也增加了0.13 e,与表面间的静电作用力增加。所以,水分子有助于LHDJ在Na-001表面吸附。
当水分子加入None-001表面后,LHDJ在表面的吸附构型变化较小。第2个水分子与第1个水分子以氢键相连,同时与LHDJ形成一个较强的氢键(布居值为0.04),增强LHDJ的吸附强度。同时LHDJ与表面形成了5个氢键,正电荷也增加了0.12 e。氢键的形成、水分子的桥联作用和静电作用力的增大都使LHDJ在None-001表面吸附的更牢固。M(None-001)L-1(-392.03 kJ/mol)和M(None-001)W(-55.30 kJ/mol)的吸附能绝对值之和447.33 kJ/mol,远小于系统M(None-001)LW的吸附能绝对值514.23 kJ/mol,说明整个体系的能量减少,有利于LHDJ的吸附。
在M(Inter)LW构型中,LHDJ与下表面形成3个氢键,键长分别为2.151×10-10,2.030×10-10和2.368×10-10 m,同时H2O桥接LHDJ和下表面,与表面形成一个氢键,键长为2.374×10-10 m,这样LHDJ与上下内表面的吸附更加牢固,体系的能量也进一步降低了。M(Inter)LW系统吸附能的绝对值为780.29 kJ/mol,大于其子系统M(Inter)L-1和M(Inter)W的吸附能绝对值之和739.81 kJ/mol。
2.3 LHDJ抑制蒙脱石水化膨胀机理的讨论
由以上分析可知,LHDJ主要通过3个方式抑制蒙脱石水化膨胀:首先,LHDJ在水溶液中产生大量正电离子,中和蒙脱石表面的电负性,减弱蒙脱石表面的静电斥力;同时,LHDJ可以牢固地吸附在蒙脱石外表面,随LHDJ吸附量的增加,阻碍了水分子在表面的吸附,由LHDJ和水分子的协同吸附可知LHDJ不改变蒙脱石的亲水性;此外,由于LHDJ分子量小,易进入层间交换出钠离子,依靠静电作用、氢键作用和水分子的桥联与上下两表面发生吸附,拉紧层间距,抑制了水分子进入层间从而导致的层间增大。
3 结 论
(1)LHDJ在蒙脱石001表面和层间都能稳定吸附,但LHDJ在Na-001表面吸附主要是静电作用,在None-001表面和层间的吸附是氢键和静电引力的共同作用。Na离子在Na-001表面的存在阻碍了LHDJ与表面间的电子转移以及氢键的形成,不利于LHDJ在表面的吸附。
(2)水分子的存在加强了LHDJ在蒙脱石表面的吸附,LHDJ与水分子展现出协同吸附效应,水分子桥联LHDJ与蒙脱石表面并增强它们之间的静电作用和氢键作用。
(3)LHDJ主要通过3个方式抑制蒙脱石水化膨胀:首先,LHDJ在水溶液中产生大量正电离子,中和蒙脱石表面的电负性,减弱蒙脱石表面的静电斥力;同时,LHDJ可以牢固地吸附在蒙脱石外表面,随LHDJ吸附量的增加,阻碍了水分子在表面的吸附,但并不改变蒙脱石的亲水性;此外,LHDJ易进入层间交换出钠离子,依靠静电作用、氢键作用和水分子的桥联作用与上下表面吸附牢固,拉紧层间距,水分子不易进入层间增大层间距。
参考文献(References):
[1] 刘长武,陆士良.泥岩遇水崩解软化机理的研究[J].岩土力学,2000,21(1):28-31.
LIU Changwu,LU Shiliang.Research on mechanism of mudstone degradation and softe ning in water[J].Rock and Soil Mechanics,2000,21(1):28-31.
[2] 陈秀荣.泥页岩井壁稳定性研究[D].武汉:中国地质大学,2009.
CHEN Xiurong.Study on Well-bore stability in shale formation[D].Wuhan:China University of Geosciences,2009
[3] SUN L H,WU H Y,YANG B S,et al.Support failure of a high-stress soft-rock roadway in deep coal mine and the equalized yielding support technology:A case study[J].International Journal of Coal Science & Technology,2015,4(4):279-286.
[4] 杨林青.矸石泥化抑制的规律及机理研究[D].徐州:中国矿业大学,2014.
YANG Linqing.The regularity and mechanism researsh of inhibiting the dispersion of gangue[D].Xuzhou:China University of Mining and Technology,2014.
[5] 王冉.黏土泥化抑制对煤泥浮选的影响[D].徐州:中国矿业大学,2015.
WANG Ran.The effect of inhibiting clay dispersion on coal flotation[D].Xuzhou:China University of Mining and Technology,2015.
[6] 余娇梅,张亚博,胡三清.小阳离子粘土稳定剂的合成与性能评价[J].长江大学学报,2008,5(2):26-28,137-138.
YU Jiaomei,ZHANG Yabo,HU Sanqing.Systhesis of mini-cationic clay stabilizer and its performance evaluation[J].Journal of Yangtze University,2008,5(2):26-28,137-138.
[7] 刘晓明.小阳离子黏土防膨剂的应用性能研究[D].济南:山东大学,2012.
LIU Xiaoming.Research on small cationic clay anti-swelling agent application performanc[D].Jinan:Shandong University,2012.
[8] 崔岩.小阳离子黏土稳定剂结构设计及性能评价[D].天津:天津科技大学,2011.
CUI Yan.Structure design and performance evaluation of small cationic clay stabilizers[D].Tianjin:Tianjin University of Science and Technology,2011.
[9] EL-MONIER E A,NASR-EL-DIN H A.A study of several environmentally friendly clay stabilizers[A].SPE Project and Facilities Challenges Conference at METS.Soliety of Petroleum Engineers,2011.
[10] LI Y,CHEN J,KANG D,et al.Depression of pyrite in alkaline medium and its subsequent activation by copper[J].Minerals Engineering,2012,26(1):64-69.
[11] 郗朋,刘文礼,杨宗义,等.基于量子化学的碳原子吸附对煤系黄铁矿表面疏水性影响的研究[J].煤炭学报,2017,42(5):1290-1296.
XI Peng,LIU Wenli,YANG Zongyi,et al.Influence of carbon atom adsorption on coal pyrite hydrophobicity based on quantum chemistry[J].Journal of China CoaSociety,2017,42(5):1290-1296.
[12] 陈军,闵凡飞,刘令云,等.不同胺/铵阳离子在高岭石(001)面吸附的密度泛函计算[J].煤炭学报,2016,41(12):3115-3121.
CHEN Jun,MIN Fanfei,LIU Lingyun,et al.DFT calculations of different amine/ammonium cations adsorption on kaolinite(001) surface[J].Journal of China Coal Society,2016,41(12):3115-3121.
[13] 韩永华,刘文礼,陈建华,等.羟基钙在高岭石两种(001)晶面的吸附机理[J].煤炭学报,2016,41(3):743-750.
HAN Yonghua,LIU Wenli,CHEN Jianhua,et al.Adsorption mechanism of hydroxyl calcium on two kaolinite (001) surface[J].Journal of China Coal Society,2016,41(3):743-750.
[14] SHI J,LIU H,MENG Y,et al.First-principles study of ammonium ions and their hydration in montmorillonites[J].Journal of Molecular Modeling,2013,19(4):1875-1881.
[15] VOORA V K,ALSAIDI W A,JORDAN K D.Density functional theory study of Pyrophyllite and M-Montmorillonites (M=Li,Na,K,Mg,and Ca):Role of dispersion interactions[J].Journal of Physical Chemistry A,2011,115(34):9695.
[16] PERDEW J P,BURKE K,ERNZERHOF M.Generalized gradient approximation made simple[J].Physical Review Letters,1996,77:365-3868.
[17] ZHANG G,ALSAIDI W A,MYSHAKIN E M,et al.Dispersion-corrected density functional theory and classical force field calculations of water loading on a pyrophyllite(001) surface[J].Journal of Physical Chemistry C,2012,116(32):17134-17141.
[18] PENG C,MIN F,LIU L,et al.A periodic DFT study of adsorption of water on sodium-montmorillonite (001) basal and (010) edge surface[J].Applied Surface Science,2016,387:308-316.
[19] SCHOLTZOV E,TUNEGA D,MADEJOV
E,TUNEGA D,MADEJOV J,et al.Theoretical and experimental study of montmorillonite intercalated with tetramethylammonium cation[J].Vibrational Spectroscopy,2013,66(5):123-131.
J,et al.Theoretical and experimental study of montmorillonite intercalated with tetramethylammonium cation[J].Vibrational Spectroscopy,2013,66(5):123-131.
[20] SHI J,LOU Z,YANG M,et al.An interlayer expansion model for counterion-intercalated montmorillonite from first-principles calculations[J].Computational Materials Science,2015,96(96):134-139.
[21] PENG C,MIN F,LIU L,et al.The adsorption of CaOH+on (001) basal and (010) edge surface of Na-montmorillonite:A DFT study[J].Surface & Interface Analysis,2017,49:267-277.