马双忱1,柴 晋1,万忠诚2,武 凯1,张净瑞2,陈嘉宁1
(1.华北电力大学 环境科学与工程学院,河北 保定 071003; 2.盛发环保有限公司,福建 厦门 361000)
摘 要:随着国家“水污染防治行动计划”政策的提出,脱硫废水零排放已成为电厂水污染深度治理的新趋势。针对高温烟气蒸发脱硫废水技术应用中面临的核心技术问题,即不同工况条件下氯离子气相转化特性问题开展模型及实验研究。将经典的气液相平衡理论应用于复杂的脱硫废水混盐体系,基于状态方程法计算得出理想体系中以温度为自变量的氯离子气固相分配系数模型。之后,将得出的理想模型用复杂体系废水即脱硫废水进行验证和线性修正,引入修正系数ε和修正常数φ。利用自行设计的实验台开展实验研究,分析各个影响因素对氯离子气固相分配的显著性,影响最大的因素为温度,其次是pH和氯离子浓度,脱硫废水中所含的主要阳离子影响最大的是Mg2+,其次是Ca2+和Na+。得出的实际废水和正交实验数据用以拟合数据,确定了修正系数ε=1.068,修正常数φ中包含了上述影响氯离子气相转化的关键环境参数和水质参数。以MATLAB为计算工具对数据进行拟合,选取指数、对数及线性函数3种拟合形式,其中线性拟合的相关性最高,拟合度R2为0.925 8,达到拟合要求。得到了适用于180~380 ℃的氯离子气固相分配系数模型。研究结果为脱硫废水烟气蒸发技术的应用提供了关键数据,实现了对脱硫废水蒸发过程中氯离子挥发量的量化及预测,可为该技术的工程实践提供参考。
关键词:脱硫废水;烟气蒸发;氯挥发;气固相分配
中图分类号:X703
文献标志码:A
文章编号:0253-9993(2019)04-1247-08
收稿日期:2018![]() 04
04![]() 20
20
修回日期:2018![]() 12
12![]() 12
12
责任编辑:毕永华
基金项目:华北电力大学中央高校基金资助项目(2017XS124)
作者简介:马双忱(1968—),男,辽宁大连人,教授,博士生导师。E-mail:msc1225@163.com
MA Shuangchen1,CHAI Jin1,WAN Zhongcheng2,WU Kai1,ZHANG Jingrui2,CHEN Jianing1
(1.School of Environmental Science and Engineering,North China Electric Power University (Baoding),Baoding 071003, China; 2.Shengfa Environmental Protection Co.,Xiamen 361000,China)
Abstract:Since the promulgation of “water pollution control action plan” in China,a zero liquid discharge of desulfurization wastewater has become a new trend of water pollution control in power plant.Aiming at the core technical issue on the application of desulfurization wastewater evaporation technology using high temperature flue gas,the modeling and experimental research on the gas-phase conversion characteristics of chloride ion under different operation conditions were carried out in this paper.The traditional gas-liquid equilibrium theory was applied to the complex mixed salt system.Based on state equation,the model of chloride ion gas-solid phase partition coefficient in ideal system was calculated.The ideal model was validated and linearly corrected with complex water namely desulfurization wastewater by correction factor ε and correction constant φ.Then,experimental research was conducted using self-designed device.The interaction and significance of each factor were compared and analyzed.The order of influence significance on chloride ion gas-solid distribution coefficient is temperature>pH>Cl- concentration>Mg2+ concentration>Ca2+ concentration>Na+ concentration.The correction factor is determined using real desulfurization wastewater and orthogonal experimental data ε= 1.068.The correction constant φ contains key environmental parameter like temperature and water quality parameters that affect the gas phase conversion of chloride ion.MATLAB was used to calculate the models,three fitting forms were selected and the linear fitting had the highest correlation R2=0.925 8 that meets with requirement.Finally,the model of chlorine ion gas-solid phase partition coefficient suitable for the temperature range from 180 to 380 ℃ was obtained.The study provides key data for the application of high temperature flue gas evaporation technology,obtains the quantification and prediction of chloride ion volatilization during desulfurization wastewater evaporation.The research results provide an important theoretical and practical reference for the application of this technology.
Key words:desulfurization wastewater;flue gas evaporation;HCl volatilization;gas-solid phase partition
马双忱,柴晋,万忠诚,等.脱硫废水烟气蒸发过程中氯离子气固相分配模型及实验研究[J].煤炭学报,2019,44(4):1247-1254.doi:10.13225/j.cnki.jccs.2018.0536
MA Shuangchen,CHAI Jin,WAN Zhongcheng,et al.Model and experimental research on gas-solid phase partition of chloride ion in the process of desulfurization wastewater evaporation using flue gas[J].Journal of China Coal Society,2019,44(4):1247-1254.doi:10.13225/j.cnki.jccs.2018.0536
2015-04-16,国务院发布了《水污染防治行动计划》[1],国家将强化对各类水污染的治理力度,脱硫废水为电厂的终端废水,水质恶劣,成分复杂,脱硫废水零排放成为电厂水污染深度治理的首要任务;2017-06-01,环保部印发《火电厂污染防治可行性技术指南》[2],明确提出了烟气蒸发干燥、热法结晶工艺进行废水近零排放的技术路线。
在众多零排放技术路线中,高温烟气蒸发技术受到普遍关注[3],该技术从SCR后、空预器前抽取干燥过程所需的热烟气,经雾化器雾化的脱硫废水以细小液滴的形式和热烟气在烟道内相互接触、传质传热,完成干燥过程,蒸发产物与烟气一起返回原烟道进入除尘器,蒸发产物随粉尘一起被捕集,但脱硫废水蒸发过程中会释放部分气态HCl,而除尘器对气态物质去除效率极低[4-6],该部分气态HCl将进入脱硫系统,无疑会影响脱硫系统的氯平衡和水平衡,当氯挥发量过大时,会增加脱硫废水排放量;另外,浆液中Cl-浓度过高对石膏品质、脱硫系统腐蚀和脱硫效率等也会产生不利影响[7-9]。在废水零排放的发展趋势下,如何量化及预测不同工况条件下氯挥发量,建立氯离子气固相分配模型成为了脱硫废水高温烟气蒸发技术的核心问题。
关于氯离子的相间分配模型,目前主要有活度系数法和状态方程法2种研究手段[10-14],国外学者主要利用活度系数法计算氯的气液相分配,定义气液相分配系数KD,即
(1)
其中,mclvap为气相Cl-浓度;mclliq为液相Cl-浓度;γclliq为氯离子液相活度系数。J M SIMOMSON[15]探究了50~350 ℃温度条件下氯离子的气液相分配规律,首次提出式(2)氯离子的气液相分配经验模型,同时提出氯离子的气液相分配受到溶液温度、pH、氯离子含量、含盐量及盐成分等多方面因素影响[16]。
(2)
其中,T为蒸发温度;ρw为水的密度;A,B,C和D为分配常数。M S GRUSZKIEWICZ[17-19]和LIU C K[20]将上述理论研究与电厂锅炉水高温高压工况下的溶解携带理论[21-22]相结合,得出式(3)关于温度的简化模型,即氯离子气液相分配系数的对数与温度的倒数成正比。
(3)
式中,Tc,HCl和ρc,HCl分别为HCl的临界温度和临界密度;ρw为水的密度;A和B为分配常数。
一般状态下氯离子通常是以HCl和NH4Cl的形式挥发到气相,在低氨浓度时,以HCl的形式为主[18],脱硫废水中NH4+平均含量为9.39 mg/L,属于低氨水质;Otakar JONAS[23]研究了纯水的pH随温度的变化,纯水的pH随温度的升高呈现出降低的趋势,在430 ℃时达到最低pH为5.6,也就是说,水在高温下有“酸化”的倾向,当水中含有Cl-时,水解离生成的H+易与Cl-结合,以气态HCl的形式挥发溢出,另外NaCl,CaCl2,MgCl2等可能在高温条件下水解生成气态HCl。氯离子挥发机理总结如下[18,23-24]:
H2O![]() H++OH-,H++Cl-=HCl↑
H++OH-,H++Cl-=HCl↑
(1)
NaCl+2H2O![]() NaOH+HCl↑
NaOH+HCl↑
(2)
CaCl2+2H2O![]() Ca(OH)2+2HCl↑
Ca(OH)2+2HCl↑
(3)
MgCl2+2H2O![]() Mg(OH)2+2HCl↑
Mg(OH)2+2HCl↑
(4)
反应(1)为氯离子气相转化的主要形式,反应(2)~(4)可能在蒸发温度较高时发生,且反应强度不高。
笔者以脱硫废水蒸发过程为研究对象,将传质分离过程中涉及的气液相平衡理论和状态方程法应用于复杂的混盐体系,并根据实验数据加以修正,得出适用于180~380 ℃温度条件且包含关键影响因素的氯离子气固相分配系数计算模型,实现了对脱硫废水蒸发过程中氯挥发量的量化及预测,为脱硫废水烟气蒸发技术的应用提供了重要的数据支持,有重要的理论和实用价值。
图1为不同体系氯离子的气固相分配机理示意图,模型简化及假设如下:
(1)由上述研究进展可知,在低氨浓度时,氯离子主要以HCl的形式挥发到气相,且纯水pH随温度升高而降低,水解离的H+易与Cl-结合,以气态HCl的形式溢出,脱硫废水属于低氨酸性水质,所以,理论模型计算时定义理想状态,假设理想状态下氯离子全部以HCl的形式挥发到气相;
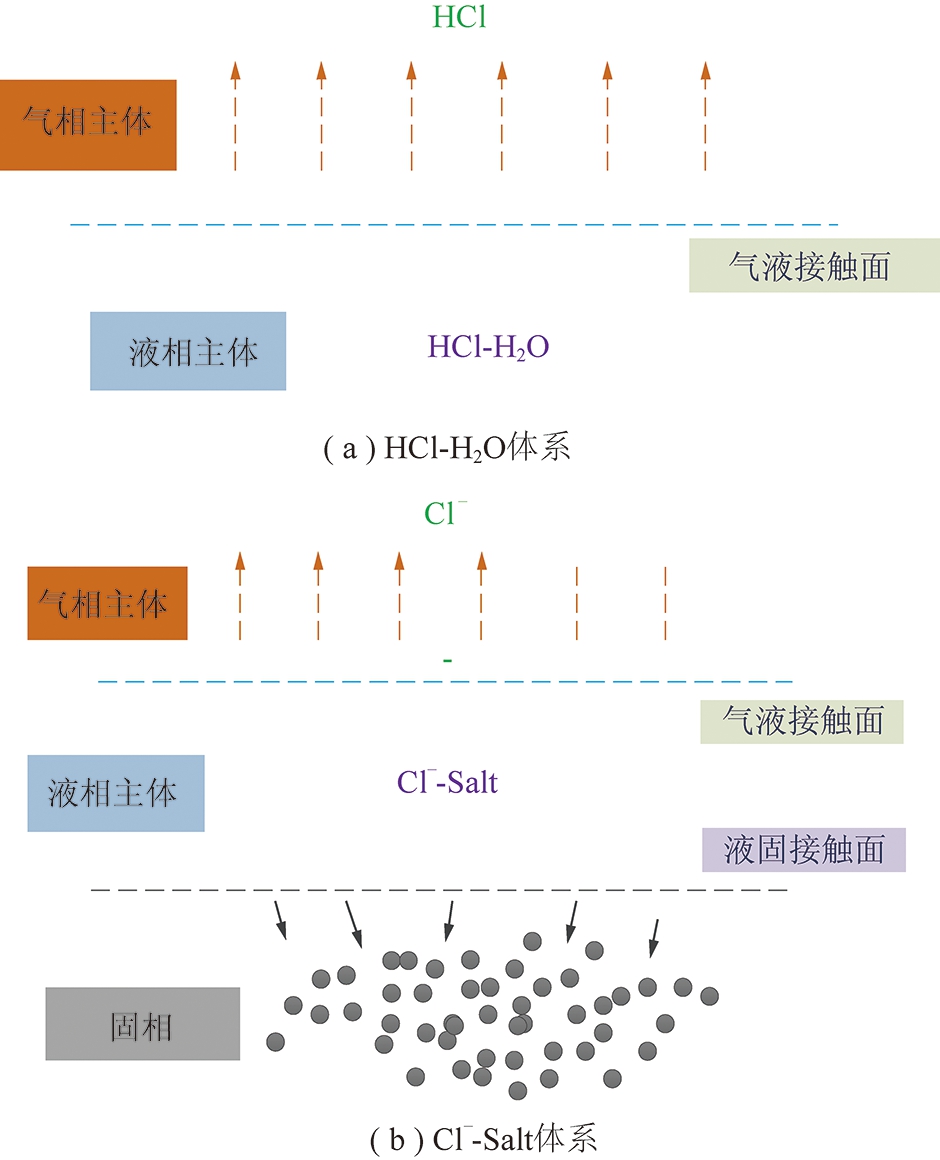
图1 不同体系氯离子气固相分配机理
Fig.1 Gas-solid phase partition mechanism of chloride ions in different systems
(2)将氯离子在理想状态下的挥发简化为HCl-纯水体系(以下简称HCl-H2O体系),如图1(a)所示,在蒸发过程中HCl和H2O的传质传热分离过程,在探究脱硫废水等复杂体系时,将理想状态替换为实际的Cl--混盐体系(以下简称Cl--Salt体系),如图1(b)所示,并对HCl-H2O体系得出的理想模型加以修正;
(3)蒸发过程中传质传热分离只在气液相接触面处进行,忽略其他散热损失。
气液相平衡时,组分i在气液两相的逸度相等[25-27],即
(4)
其中,上标V和L分别表示气相和液相。逸度的计算通常引入逸度系数和活度系数。气相中组分i的逸度系数![]() 定义为
定义为
(5)
式中,p为总压;yi为气相组分i的摩尔分率,同理可得液相中组分i的逸度系数:
(6)
其中,xi为液相中组分i的摩尔分率。将式(5),(6)代入式(4)中得到
(7)
则气液相分配系数可表示为
(8)
式中,逸度系数可通过状态方程来计算,常用的以V和T作为独立变量,导出计算逸度系数的普遍化方程:
其中,Vm,t为气(液)相混合物的总体积;Zm为气(液)相混合物的压缩因子;ni为组分i的物质的量。但通过式(9)并不能直接得到数值解,本文采用Van Der Waals提出的实际气体状态方程[28-29]:
(10)
Van Der Waals方程,引入了a,b两项气相混合物范德华常数,a是分子间引力对p的校正,b为分子本身的体积校正,结合经典的VDW混合规则,可以推导出可迭代计算的气、液两相逸度系数的表达式:
(11)
式中,ai,bi为气相组分i的范德华常数,a,b由下式计算:
(12)
![]()
(13)
用式(14)~(15)计算总体积Vm,t和压缩因子Zm:
(14)
![]()
(15)
其中,Tc,i为组分i的临界温度;pc,i为组分i的临界压力。将上述结果代入逸度系数表达式(11)即可求得气相、液相逸度系数。
以温度T为变量,计算180~380 ℃温度范围的KHCl和KH2O,定义氯离子气固相分配系数为KHCl和KH2O的比值,得到HCl-H2O体系条件下氯离子气固相分配系数:
(16)
Cl--Salt体系条件下氯离子气固相分配系数:
(17)
式中,ε为修正系数;φ为修正常数。
以上模型通过Matlab计算得到拟合度最高的HCl-H2O体系条件下氯离子气固相分配系数模型如图2所示,模型表达式为
lg KHCl-H2O=0.716 3e0.002 3T
(18)
上述模型(18)为理想状态下得出的,当用于脱硫废水等复杂的Cl--Salt体系时需要通过实验验证并予以修正。引入修正系数和修正常数对HCl-H2O
体系模型进行线性修正,形式如下:
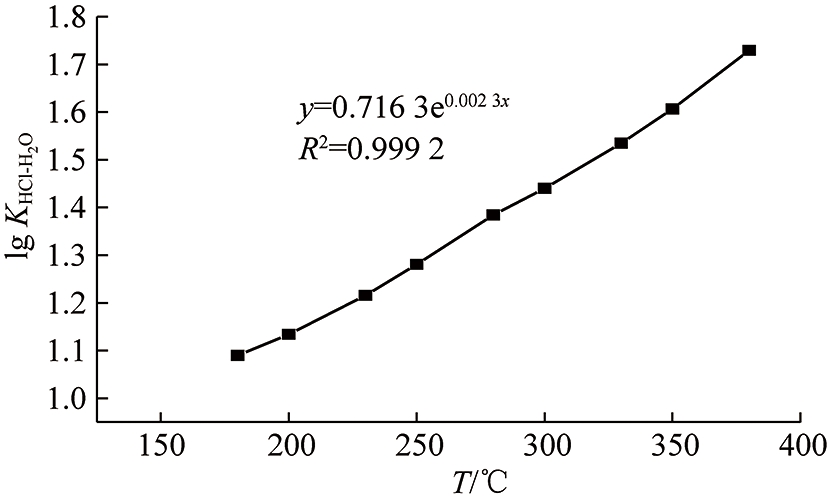
图2 HCl-H2O体系条件下氯离子气固相分配系数模型
Fig.2 Model of chloride ions gas-solid phase partition in HCl-H2O system
(19)
式中,CCl-vap为气相挥发的氯浓度;CCl-Total为液相氯的总浓度。
若确定了ε与φ的值或表达式,则实现了对于蒸发过程中氯离子气固相分配系数的量化及预测。
氯离子气固相分配系数测定系统如图3所示,每次量取等量的样品溶液置于坩埚中并在恒温干燥箱中加热;空压机产生的空气经加热管加热后引入恒温箱中的密封玻璃罩,恒温箱进出气用玻璃棉保温;实验系统尾部的真空泵将蒸干后的气体抽送至孟氏洗瓶,挥发出的气态氯化物被洗瓶中的NaOH溶液吸收,二级洗瓶内为AgNO3,用以监测一级洗瓶吸收气相Cl-是否完全,将洗瓶置于恒温水浴维持吸收温度恒定,剩余气体排空,整个实验过程通过调节流量计维持空压机进气与真空泵排气处于动态平衡;利用皖仪IC6000离子色谱对洗气瓶内吸收液中溶解的Cl-进行定量分析,实验控制条件见表1。
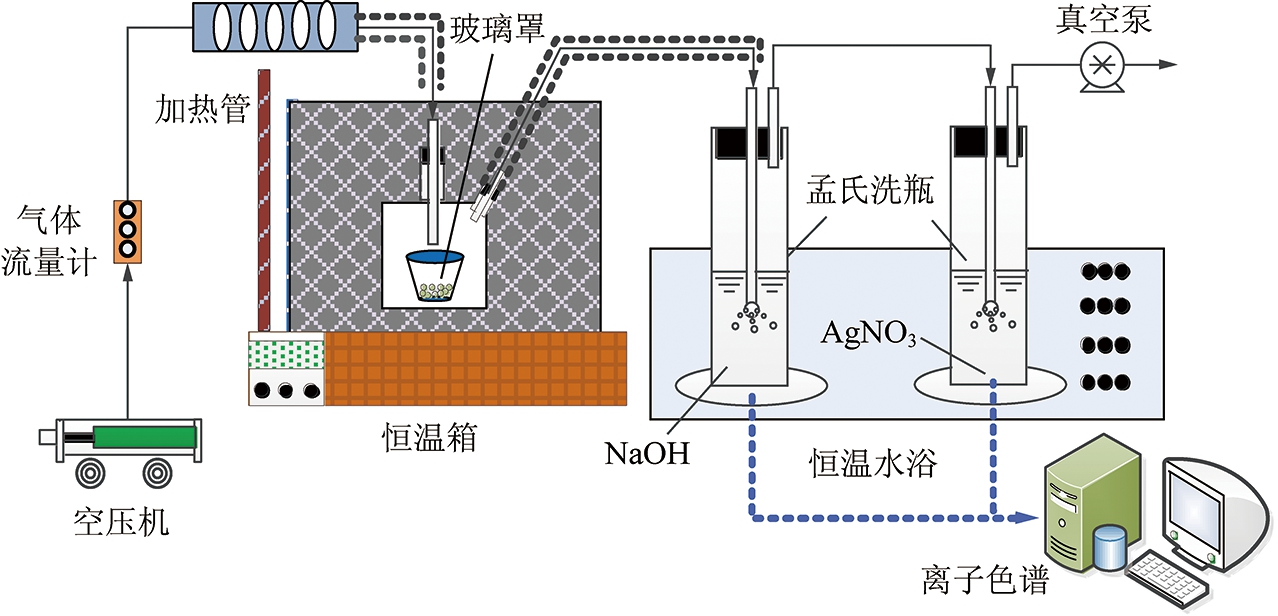
图3 氯离子气固相分配系数测定系统
Fig.3 Measuring system of chloride ion gas-solid phase partition coefficient
表1 实验条件参数
Table 1 Parameters of experimental condition
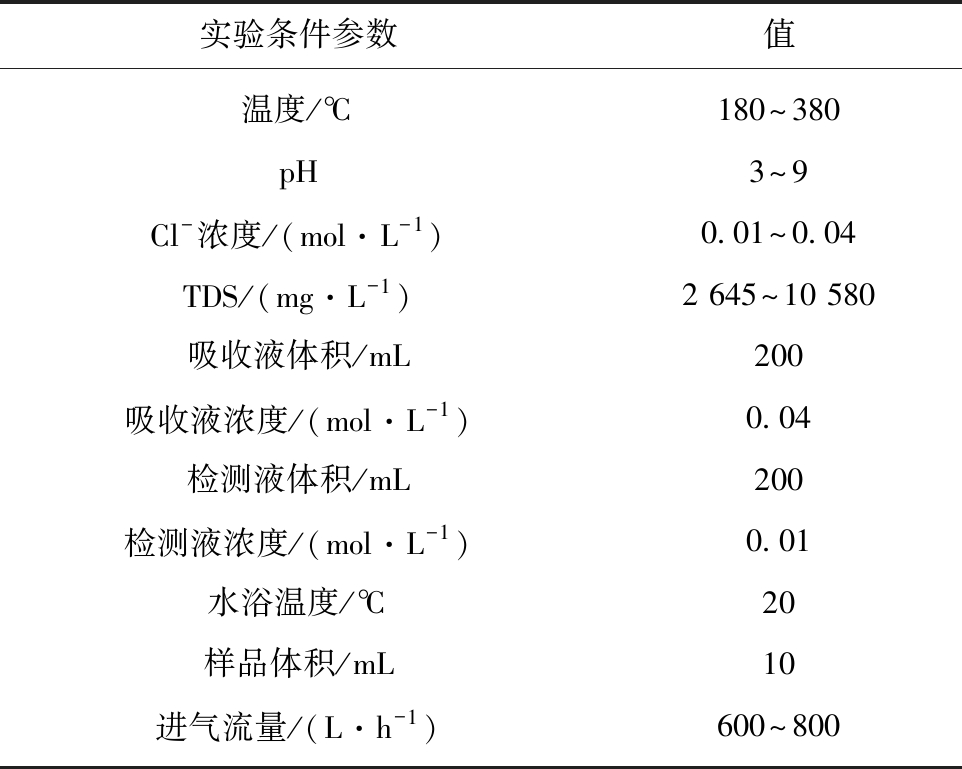
用于计算并Cl--Salt体系内氯离子气固相分配系数模型中修正系数,验证模型适用性的样品溶液分别为两个电厂的脱硫废水,部分水质参数见表2。
水样1和水样2中所含Cl-浓度用CTotal表示,按上述实验方法,分别在180,200,230,250,280,300,330,350,380 ℃温度条件下蒸干水样1和水样2。
图4为水样1和水样2在不同温度条件下的氯离子气固相分配系数曲线与理想HCl-H2O体系模型拟合后得到的线性修正关系,拟合方程表明,Cl--Salt体系与HCl-H2O体系计算出的理论模型有良好的线性关系,拟合度![]() 为
为![]() 达到0.974 7,且修正系数ε1和ε2分别为1.068 1和1.067 9,相差很小,但φ1与φ2有一定偏差,以上拟合规律说明,HCl-H2O体系理论模型经过修正后适用于Cl--Salt体系,且修正系数ε可以近似取定值1.068,但修正常数受样品溶液水质影响较大,无法取得固定值。
达到0.974 7,且修正系数ε1和ε2分别为1.068 1和1.067 9,相差很小,但φ1与φ2有一定偏差,以上拟合规律说明,HCl-H2O体系理论模型经过修正后适用于Cl--Salt体系,且修正系数ε可以近似取定值1.068,但修正常数受样品溶液水质影响较大,无法取得固定值。
表2 样品溶液水质参数
Table 2 Water quality parameters of sample
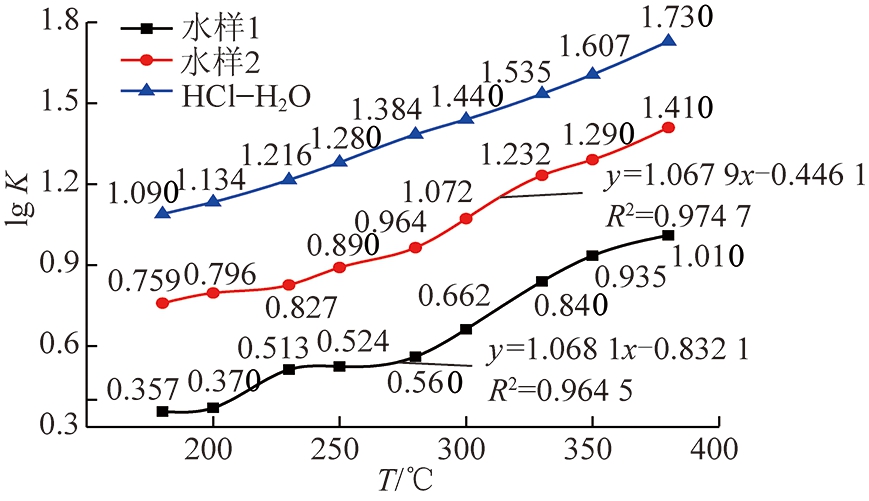
图4 lg KCl--Salt与lg KHCl-H2O的线性修正关系
Fig.4 Linear correction of lg KCl--Salt and lg KHCl-H2O
针对影响氯离子气相转化的关键环境参数,如温度,水质参数pH,Cl-浓度,Na+,Ca2+和Mg2+六个因素,设计“六因素四水平”正交实验,分析各个影响因素对氯离子气固相分配的显著性。利用上述图3实验系统得出正交实验结果见表3。
K为均值,R为极差,从R值的大小可以看出各因素对氯离子气固相分配系数影响的显著性顺序:R1(0.781)>R2(0.611)>R3(0.366)>R6(0.211)>R5(0.079)>R4(0.03),则对其影响最大的因素为温度,其次是pH,Cl-浓度,水中所含阳离子影响最大的是Mg2+,其次是Ca2+,Na+最小,相对温度和pH这两个因素而言,其余均为次要因素。
以正交实验的32组实验数据作为源数据,在Matlab中利用nlinfit多元非线性回归函数和regress多元线性回归函数对3种形式的氯离子气固相分配系数经验模型进行拟合计算。图5为3种不同形式的模型结果,结果表明,拟合度R2(1)=0.815 8,R2(2)=0.808 3,模型3的拟合度R2(3)最高,达到0.925 8,说明模型可信,满足计算要求。
利用regress函数确定模型内参数,得到氯离子气固相分配系数模型:
0.110 1pH-11.35[Cl-]-7.7[Na+]+4.39[Ca2+]+1.94[Mg2+]
(20)
用上述模型(20)的第1项和第2项减去模型(19)的第1项,并分别代入T=200,250,300和350 ℃,得到以温度T为自变量的一次函数,将该项定义为温度校正项,拟合其形式如图6所示。最终的氯离子气固相分配系数模型为
(21)
表3 正交实验结果
Table 3 Results of orthogonal experimental
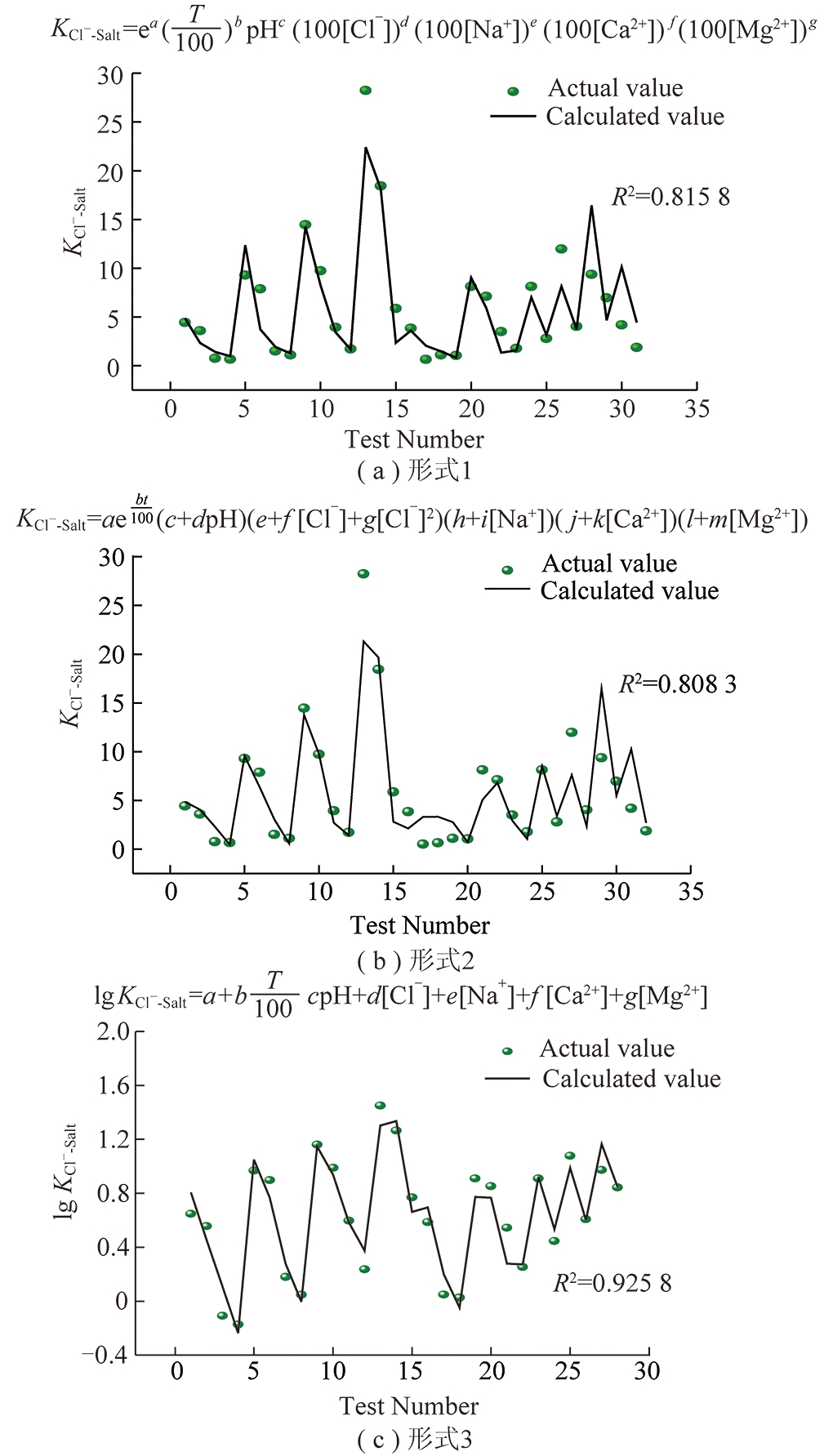
图5 不同形式公式的拟合情况
Fig.5 Fitting results of different forms of model
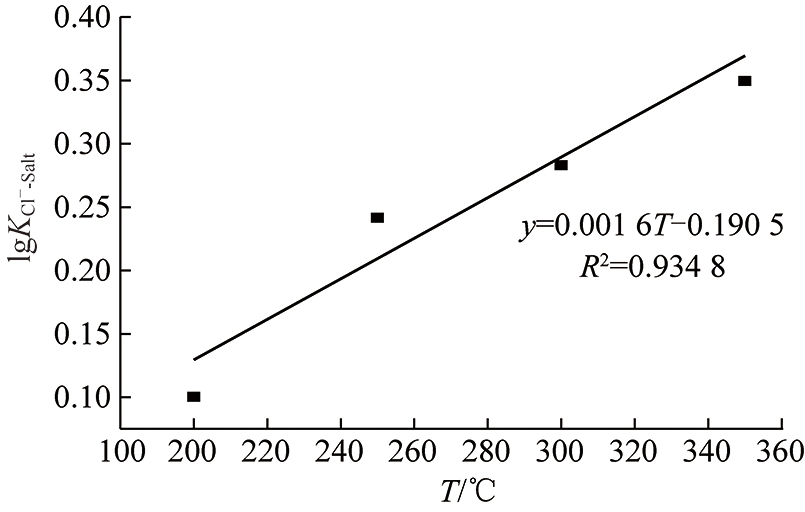
图6 温度校正项拟合
Fig.6 Fitting of temperature correction term
φ=0.001 6T-0.190 5-0.110 1pH-11.35×
[Cl-]-7.7[Na+]+4.39[Ca2+]+1.94[Mg2+]
lg KHCl-H2O=0.716 3e0.002 3T
(22)
表4为计算得出氯离子异相分配系数与其他类似研究测定的结果比较。通过表4的比较可以看出,本实验针对的是氯离子的气固相分配,而其他研究对象为气液相;相比之下,模型适用的最低温度适中,最高温度有所提高,另外,更重要的一点是,其他研究除温度变量外,修正项使用的是液相主体的密度,而本研究的模型中,温度变量是融合在气液相平衡理论之内的,且修正常数包含了影响氯离子气固相分配的关键环境参数及水质参数,更适用于实际工况。
表4 氯离子异相分配系数模型对比
Table 4 Formula fitting forms and calculation equation

(1)根据经典的气液相平衡模型计算得出了理想状态下HCl-H2O理想体系中以温度为自变量的氯离子气固相分配系数模型,可以表示为方程:
lg KHCl-H2O=0.716 3e0.002 3T
(2)HCl-纯水体系理论模型线性修正后适用于180~380 ℃温度范围的Cl--混盐体系,修正后模型可表示为
经过实际废水实验得出修正系数ε可以近似取定值1.068;
(3)利用正交实验分析各个影响因素对氯离子气固相分配的显著性,影响最大的因素为温度,其次是pH和Cl-浓度,水中所含阳离子影响最大的是Mg2+,其次是Ca2+,Na+最小,并利用实验数据拟合得出包含氯离子气相转化关键影响因素的修正常数:
φ=0.001 6T-0.190 5-0.110 1pH-11.35[Cl-]-7.7[Na+]+4.39[Ca2+]+1.94[Mg2+]
参考文献:
[1] 中华人民共和国环境保护部.国务院关于印发水污染防治行动计划的通知[EB/OL].http://zfs.mep.gov.cn/fg/gwyw/201504/t20150416_299146.htm.2015-04-16.
[2] 中华人民共和国环境保护部.火电厂污染防治最佳可行技术指南[EB/OL].http://kjs.mep.gov.cn/hjbhbz/bzwb/wrfzjszc/201706/t20170609_415755.shtml.2017-06-01.
[3] MA Shuangchen,CHAI Jin,CHEN Gongda,et al.Research on FGD wastewater evaporation:Present and future perspectives[J].Renewable and Sustainable Energy Reviews,2016,58:1143-1151.
[4] MEIJ Ruud.Trace element behavior in coal-fired power plants[J].Fuel Processing Technology,1994,39(1):199-217.
[5] MEIJ Ruud.The emissions and environmental impact of PM 10,and trace elements from a modern coal-fired power plant equipped with ESP and wet FGD[J].Fuel Processing Technology,2004,85(6-7):641-656.
[6] JEMAA N,PALEOLOGOU M,THOMPSON R,et al.Chloride removal from the kraft recovery boiler ESP dust using the precipitator dust purification (PDP) system[J].Pulp and Paper Canada,1999,100(7):46-53.
[7] Pilot plant tests of chloride ion effects on wet FGD system performance,EPA-600/S7-84-039[R].USEPA,1984.
[8] CORDOBA Patricia.Status of Flue Gas Desulfurization (FGD) systems from coal-fired power plants:Overview of the physic-chemical control processes of wet limestone FGDs[J].Fuel,2015,144:274-286.
[9] SØREN Kiil,NYGAARD H,JOHNSSON J E.Simulation studies of the influence of HCl absorption on the performance of a wet flue gas desulphurisation pilot plant[J].Chemical Engineering Science,2002,57(3):347-354.
[10] MARIA dolores Gordillo,BLANCO M A,PEREYRA C,et al.Thermodynamic modelling of supercritical fluid-solid phase equilibrium data[J].Computers & Chemical Engineering,2005,29(9):1885-1890.
[11] LAZZUS Juan,RIVERA Marco.Gas-solid phase equilibrium of biosubstances by two biological algorithms[J].Revista Mexicana De Fisica,2013,59(6):577-583.
[12] STOREY J M E,LUO W,ISABELLE L M,et al.Gas/solid partitioning of semivolatile organic compounds to model atmospheric solid surfaces as a function of relative humidity.1.clean quartz[J].Environmental Science & Technology,1995,29(9):2420-2428.
[13] TSIDILKOVSKII V I,LEONIDOV I A,LAKHTIN A A,et al.High-temperature equilibrium between High-Tc oxide and gas phase[J].Physica Status Solidi (b),1991,163(1):10.
[14] LIANG Baorui,SONG Cunyi,JIA Qian,et al.Study of the desulfurization process and gas-solid-liquid phase distribution under the complex humidification conditions in dense tower[J].Advances in Environmental Protection,2012,3(4):334-339.
[15] SIMONSON J M,PALMER D A.Liquid-vapor partitioning of HCl(aq) to 350 ℃[J].Geochimica Et Cosmochimica Acta,1993,57(1):1-7.
[16] SIMONSON J M.Vapor-liquid partitioning of HCI in acidic NaCl brines at high temperatures[R].Geothermal Resources Council Transactions,1998.
[17] GRUSZKIEWICZ M S.The partitioning of acetic,formic,and phosphoric acids between liquid water and steam[R].Office of Scientific and Technical Information Technical Reports,1999.
[18] ZHOU Shengqi.Steam turbine operating conditions,chemistry of condensates,and environment assisted cracking-a critical review[R].NPL Report,2002.
[19] GUSZKIEWICZ M S.The partitioning of acetate,formate and phosphates around the water/steam cycle[R].Office of Scientific and Technical Information Technical Reports,2000.
[20] LIU Chekeung.Group-contribution methods in estimating liquid-liquid distribution coefficents[D].Lubbock:Texas Tech University,1981.
[21] BAHADOR Alireza.Prediction of silica carry-over and solubility in steam of boilers using simple correlation[J].Applied Thermal Engineering,2010,30(2-3):250-253.
[22] VLADANA N Rajakovi Ognjanovi,DRAGANA Z Živojinovic,GRGUR B N,et al.Improvement of chemical control in the water-steam cycle of thermal power plants[J].Applied Thermal Engineering,2011,31(1):119-128.
[23] OTAKAR Jonas.ESAA effective cycle chemistry control[A].Power Station Chemistry Conference[C].Rock Hampton Queensland Australia,2000.
[24] MA Shuangchen,CHAI Jin,WU Kai,et al.Experimental and model research on chloride ion gas-solid distribution in the process of desulfurization wastewater evaporation[J].RSC Advances,2018,8(46):26283-26292.
[25] SMITH J M.Introduction to chemical engineering thermodynamics[M].McGraw-Hill,1987.
[26] WALAS J M.Phase equilibria in chemical engineering[M].Boston:Butterworth Publishers,1985.
[27] CHAO Kwangchu.Thermodynamics of fluids an introduction to eq-uilibrium theroy[M].New York:Marcel Dekker Inc,1975.
[28] SCHMIDT G,WENZEL H.A modified van der Waals type equation of state[J].Chemical Engineering Science,1980,35(7):1503-1512.
[29] NHU N V,DEITERS U K.Application of a generalized van der Waals equation of state to several nonpolar mixtures[J].Fluid Phase Equilibria,1996,118(2):153-174.