煤炭是我国第一大能源,占全国能源生产和消费总量的70%以上[1]。但我国煤炭开采的自然条件相对较差,各种灾害时有发生,煤层自燃灾害就是其中之一[2]。煤炭自燃不但造成煤炭资源和采矿设备的巨大损失,而且伴随着CO,CO2,SO2等有毒有害气体的产生,严重威胁井下作业人员的人身安全。因此,煤炭自燃火灾的防治是当前煤矿安全领域亟需解决的重大课题之一。
煤炭自燃机理是研究煤炭自燃灾害防治的根本理论支撑,长期以来,国内外学者针对煤炭自燃机理开展了大量的研究,提出了多种学说,如细菌作用说、黄铁矿说、酚基作用学说和煤-氧复合作用学说等[3]。其中,由于煤-氧复合学说从宏观角度指出煤的自燃是煤氧化生热所致,较符合煤自燃发生和发展的实际现象,所以受到国内外学者的广泛认同。多年来,国内外学者采用不同的方法对煤与氧的复合过程从不同的角度开展了大量的研究。研究结果表明,煤自燃的起因是煤分子中的某些活性基团或活性结构与空气中的氧气发生了化学吸附和化学作用[4]。许多学者的研究表明,煤主要由含氧官能团、脂肪烃类和芳烃三大类官能团组成。WANG 等和LYNCH 等研究发现氧化时,煤的芳核部分是稳定的,氧原子主要攻击脂肪族基团[5-6]。王继仁和邓存宝等也指出煤氧复合过程中煤分子中的环烷烃、杂环类化合物性质稳定,不易在常温常压下与氧气发生化学反应,而其中的某些烷基侧链、桥键、和含氧官能团易于被氧化,是煤氧化放热的导因[7-8]。受此类研究结果的启发,针对煤中脂肪烃类及含氧官能团的结构与氧化特性,国内外学者开展了大量的研究[9-11]。XU等指出含氧官能团是煤氧化初期最活跃的基团[12]。杨漪利用红外拟合分峰数据及归属表明煤分子中主要含氧官能团是羟基(—OH)和羰基(—COOH)[13]。ZHANG等借助超声萃取技术,通过对比分析原煤样与萃余煤样的微观结构变化,得出在煤自燃过程中 —OH是占主导地位的官能团,对煤的质量损失和热释放贡献最大[14]。王德明等在研究煤自燃基元反应的过程中发现羟基自由基(HO·)是煤自燃链式反应中的关键性连接基团之一[15]。葛岭梅、张嬿妮等将煤分子中常温下易与氧发生反应的活性基团分为桥键和侧链两大类[16-17]。桥键类包括α位带羟基的次烷基键、次甲基醚键和两边都与芳环相连的次甲基3种。甲氧基、与芳环相连的边缘醛基和α位碳原子带羟基的烷基侧链归属于侧链类活性基团。王继仁和邓存宝等基于量子化学理论对这些活性结构的氧化反应历程进行了计算和模拟,但相关研究只模拟了部分单一活性基团的氧化反应历程,并未考虑两个或以上活性基团同时存在时的氧化反应特性,且对反应机理的推测主要基于猜测的中间产物,而没有考虑前线轨道的跃迁及电子特性[7-8]。
为此,笔者以侧链活性结构为基本单元,构建出了羟基(—OH)处于其邻位的小分子结构模型,应用量子化学理论,对其静电势分布、分子轨道、和热力学参数进行了理论计算,探究了羟基(—OH)对侧链活性基团低温氧化特性的影响,以期为煤自燃机理的研究和阻化剂的开发提供理论基础。为简化计算,笔者尚未考虑羟基(—OH)含量、位置及成键特性等因素的影响。
1 研究方法
前期研究结果表明在低温阶段,芳香环的数量对侧链和含氧官能团的性质没有明显的影响[18-22]。因此,为简化后期的计算,笔者采用简单的苯基指代煤分子中的芳香结构,以侧链活性结构 —CHO、—CHOHCH3、—OCH3为基本单元[14,16-17,23-24],构造出了羟基(—OH)处于其邻位的小分子结构模型,基于密度泛函理论(DFT),在6-311G(d,p)基组上采用B3LYP方法对搭建的煤分子简易模型进行了优化计算,构建出了如图1所示的侧链活性结构小分子模型。基于量子化学理论,对图1中所示小分子模型的静电势、前线轨道能级和电荷密度以及热力学参数进行了计算。

图1 侧链活性结构小分子模型结构
Fig.1 Molecular structures of side chain active groups
2 结果与分析
2.1 静电势与活性部位分析
图2为活性结构分子模型的静电势投影图。总体来看,煤分子中氢原子区域的电势为正(呈现蓝色),而氧原子区域的电势为负(呈红色),即煤分子的亲核反应位点在氢原子处,而亲电反应的活性位点在氧原子处[25]。
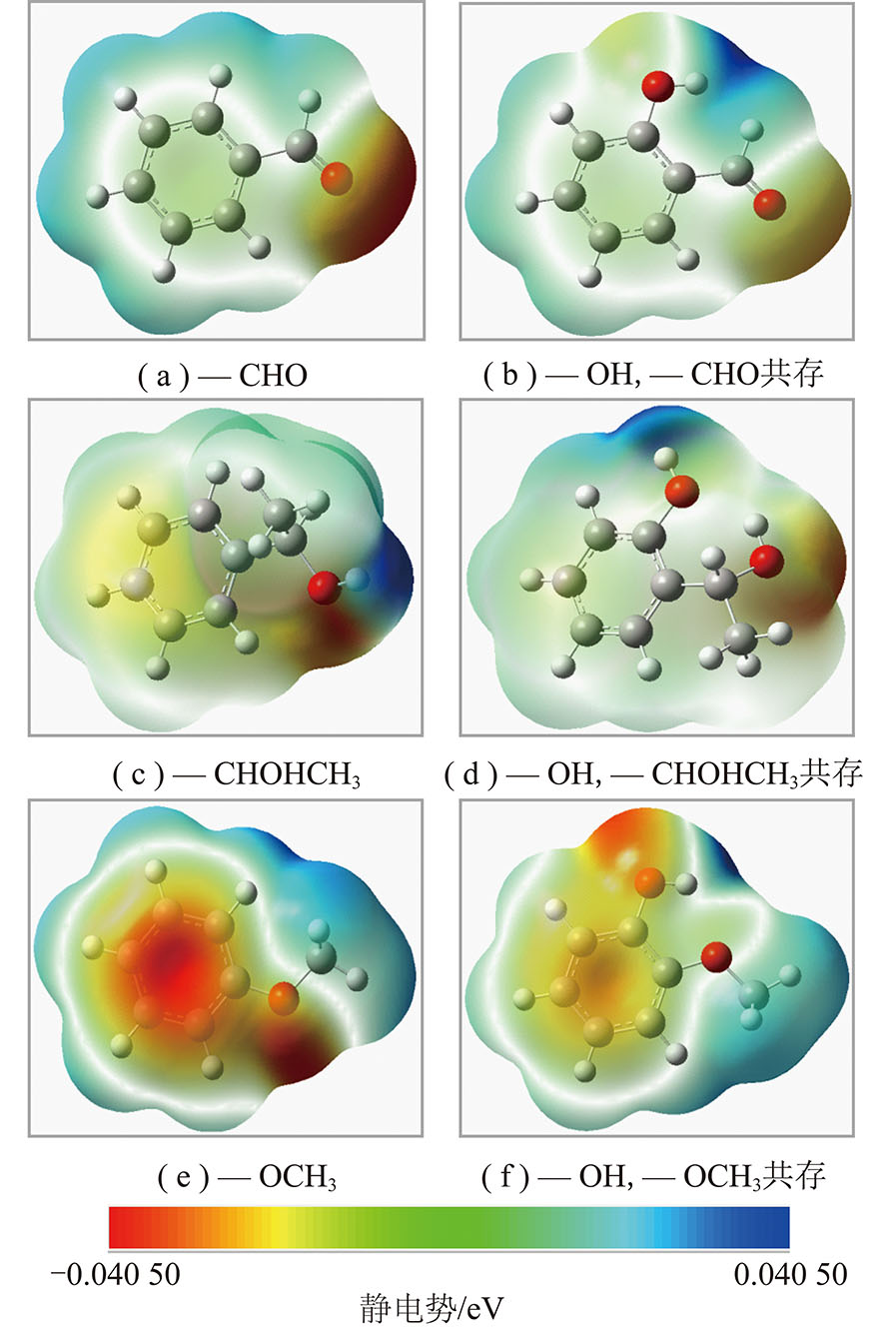
图2 小分子模型的静电势
Fig.2 Electrostatic potential maps (Red color for the negative and blue for positive charge)
图2(a),(b)显示当 —OH与侧链基团共存于煤分子中时,—CHO基团中氧原子的负电势变小(红色变浅),而氢原子附近的正电势增加(蓝色变深),表明 —OH会降低 —CHO的亲电反应能力而增加其亲核反应能力,且在煤分子多引入一个亲核反应的活性位点。由图2(c)可知,当煤分子中仅有侧链 —CHOHCH3时,—CHOHCH3中氧原子(O16)区域呈负电势,羟基氢原子(H17)的静电势有一个很大的正值。当 —OH与 —CHOHCH3共存于煤分子中时(图2(d)),O16的负电势大大降低,H17的正电势消失,表明 —OH会降低α侧链上羟基氢的亲核反应能力,并使氧原子的亲电反应能力消失。图2(e)显示,当 —OCH3单独存在时,—OCH3中的氧原子区域(O13)有一个很大的负静电势,同时 —CH3区域呈微弱的正电势,当 —OH与 —OCH3共存时(图2(f)),—OCH3基团中氧原子(O13)的正电势消失,氢原子(H14-H16)的正电势也被进一步削弱,该变化趋势表明当 —OH与 —OCH3共存于煤分子中时,—OH会削弱 —OCH3基团的亲电反应能力并使其失去亲核反应能力。
2.2 前线轨道与反应特性分析
前线轨道理论认为,化学反应的发生是由于2个反应物之间最高占位轨道(HOMO:Highest Occupied Molecular Orbital)和最低未占轨道(LUMO:Lowest Unoccupied Molecular Orbital)相互吸引,发生电子转移,进而导致反应的发生,化学反应的成键特性取决于前线轨道的能级及电荷分布[26]。LUMO与HOMO之间的能隙差越小,分子内电子的跃迁能力越强,分子稳定性越低。化学反应中,亲电反应的活性位点为被HOMO覆盖的原子,而亲核反应的活性点则为被LUMO轨道覆盖的原子,且亲核试剂最易进攻LUMO上电荷密度最大的原子[27]。氧气可被视为亲核试剂,当其与煤发生复合反应时,首先进攻的是煤分子中LUMO上电荷密度最大的原子。所以,本文对构建的小分子模型的HOMO和LUMO进行了模拟计算,分别从前线轨道的能级和LUMO上电荷密度两方面探究了 —OH对侧链活性基团氧化反应特性的影响,结果如表1、图3所示。
表1 小分子模型前线分子轨道能级
Table 1 Energies of frontier molecular orbital for constructed molecules
eV
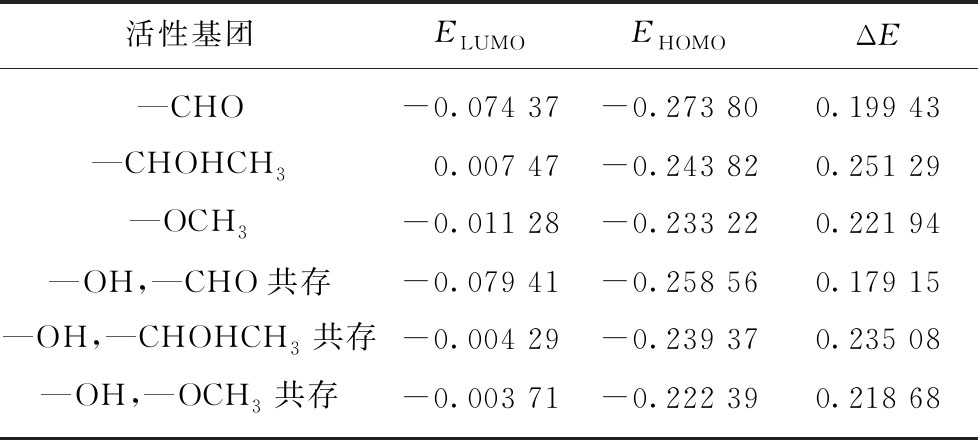
活性基团ELUMOEHOMOΔE—CHO-0.074 37-0.273 800.199 43—CHOHCH30.007 47-0.243 820.251 29—OCH3-0.011 28-0.233 220.221 94—OH,—CHO共存-0.079 41-0.258 560.179 15—OH,—CHOHCH3共存-0.004 29-0.239 370.235 08—OH,—OCH3共存-0.003 71-0.222 390.218 68
LUMO与HOMO上的能隙值(ΔE)反映了电子从占据轨道向空轨道跃迁的能力,能隙值(ΔE)越小,则说明电子越容易跃迁,反应活性越强[28]。由表1中的数据可知,当煤分子中仅有侧链活性基团时,侧链活性基团的反应活性为—CHO>—OCH3>—CHOHCH3。当 —OH与侧链基团共存时,侧链活性基团的活性次序虽保持不变,但反应活性均增强。
图3为小分子模型LUMO电子云分布图。由图3可知,当侧链活性基团单独存在时,—CHOHCH3的LUMO上电子云分布具有明显的离域特征,而—CHO的电子离域性最差,即侧链活性基团的LUMO成键能力为 —CHOHCH3 >—OCH3 >—CHO。当—OH与侧链基团共存时,—CHOHCH3的电子离域性被进一步增强,且使得 —CHOHCH3中的甲基(C13与H14-H16)和羟基氢(H18)上的电子云脱落,容易产生甲基自由基(CH3·)和氢自由基(H·)。当 —OH与 —CHO和 —OCH3共存时,电子离域性虽无明显变化,但小分子模型中增加了一个活性位点。图3(e),(f)显示,—OH与—OCH3共存时,煤氧复合的活性位点从原来的C13转移至O12,且C13上的电子云向H15迁移,使得—OCH3基团更容易产生氢自由基(H·)。
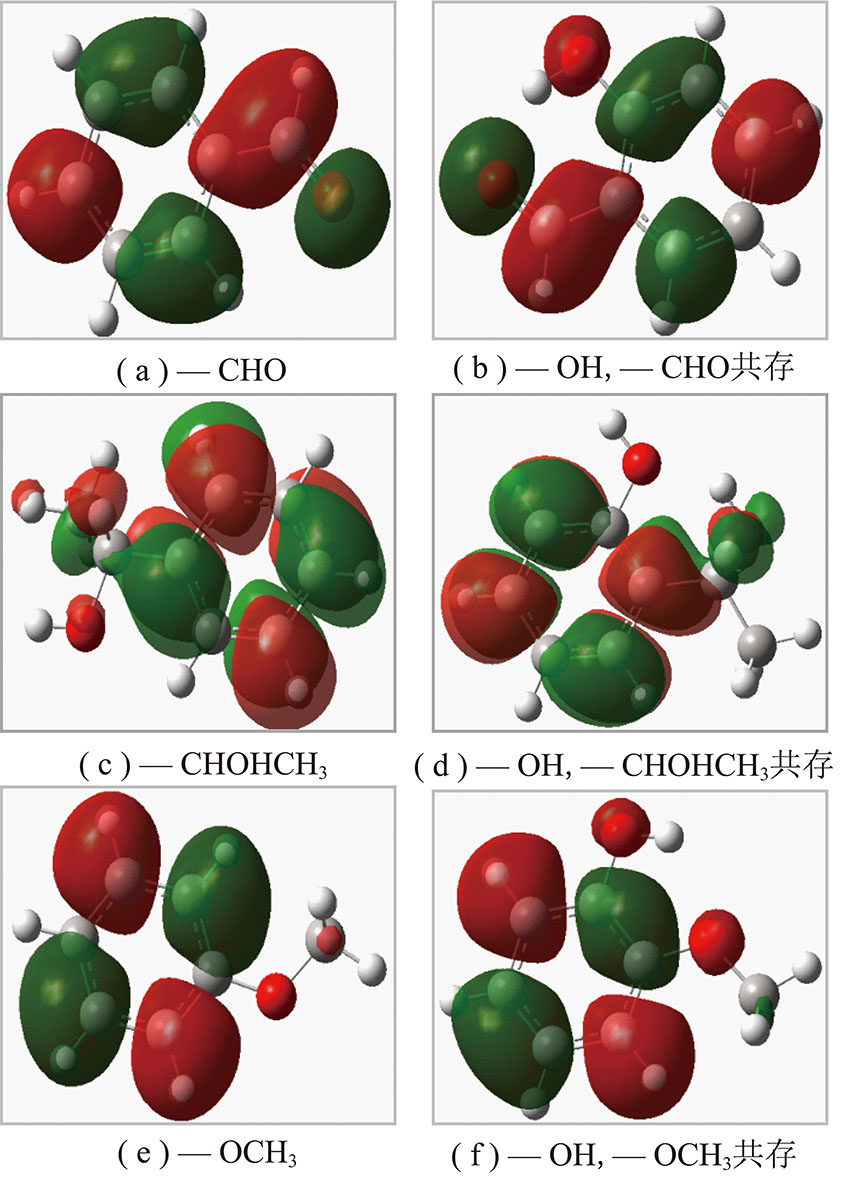
图3 小分子模型前线轨道电子云分布
Fig.3 Distribution of Frontier molecular Orbital for molecular models
2.3 热力学参数分析
焓(H)和吉布斯自由能(G)是热力学中表征物质反应活性的重要特征参数,焓变(ΔH)和其吉布斯自由能变化值(ΔG)为生成物的焓值(H)或吉布斯自由能(G)减去反应物的焓值(H)或吉布斯自由能(G)。对于任何给定的反应,当 ΔH>0时,表明该反应是吸热反应,当 ΔH<0时,该反应是放热反应,当 ΔG>0时,该反应为不可自发进行的反应,当 ΔG<0时,表示反应是自发反应[19]。基于这一理论,本文首先利用Gaussian 16计算了图1中简易煤分子中及其产物的焓值(H)和吉布斯自由能(G),计算结果见表2。
基于表2中的焓值(H)和吉布斯自由能值(G),通过量子化学计算得到了各个活性基团氧化反应的焓变(ΔH)和其吉布斯自由能变化值(ΔG),具体结果见表3。表3中,R1,R3和R7分别为侧链活性基团与氧气的复合反应。表3中的数据显示常温常压下,—CHO,—CHOHCH3和—OCH3均可自发的与氧气发生放热的复合反应,生成过氧化氢产物,因为该反应为亲核加成反应,故在宏观上应表现出煤样质量增加,与TG曲线的研究结果相符[29-31]。通过对比分析R1,R3,R7的吉布斯自由能变化值发现当仅有侧链活性基团时,其与氧气发生复合反应的活性次序为 —CHOHCH3 >—OCH3 >—CHO,与LUMO的分析结果一致,而与分子反应活性的排序结果相悖,证明煤中活性基团与氧气的复合反应能力主要取决于其LUMO的成键能力而非活性基团的反应活性。当 —OH与侧链活性基团共存时,—CHO更容易与氧气发生复合反应,但反应过程中放出的热量减少,主要是因为 —OH虽然增强了 —CHO的亲核反应能力即吸附氧气的能力,但同时在分子中又引入了一个亲核反应位点,故降低了 —OCH与氧气的反应强度。—OH使得 —CHOHCH3与氧气的反应不但更容易发生且反应更剧烈,主要是因为 —OH增强了 —CHOHCH3的LUMO上的电子离域性进而提高了其成键能力,而甲基自由基(CH3·)和氢自由基(H·)的产生又进一步提高了其链式反应的反应速率。表3中的数据显示,当 —OH处于邻位时,—OCH3与氧气的复合反应由自发的放热反应转为非自发的吸热反应,这主要归于 —OH使 —OCH3与氧复合的活性位点发生了转移,亲核反应能力消失的缘故。
表2 反应物和产物的优化结构、吉布斯自由能和焓值
Table 2 Thermodynamic parameters of reactants and corresponding products
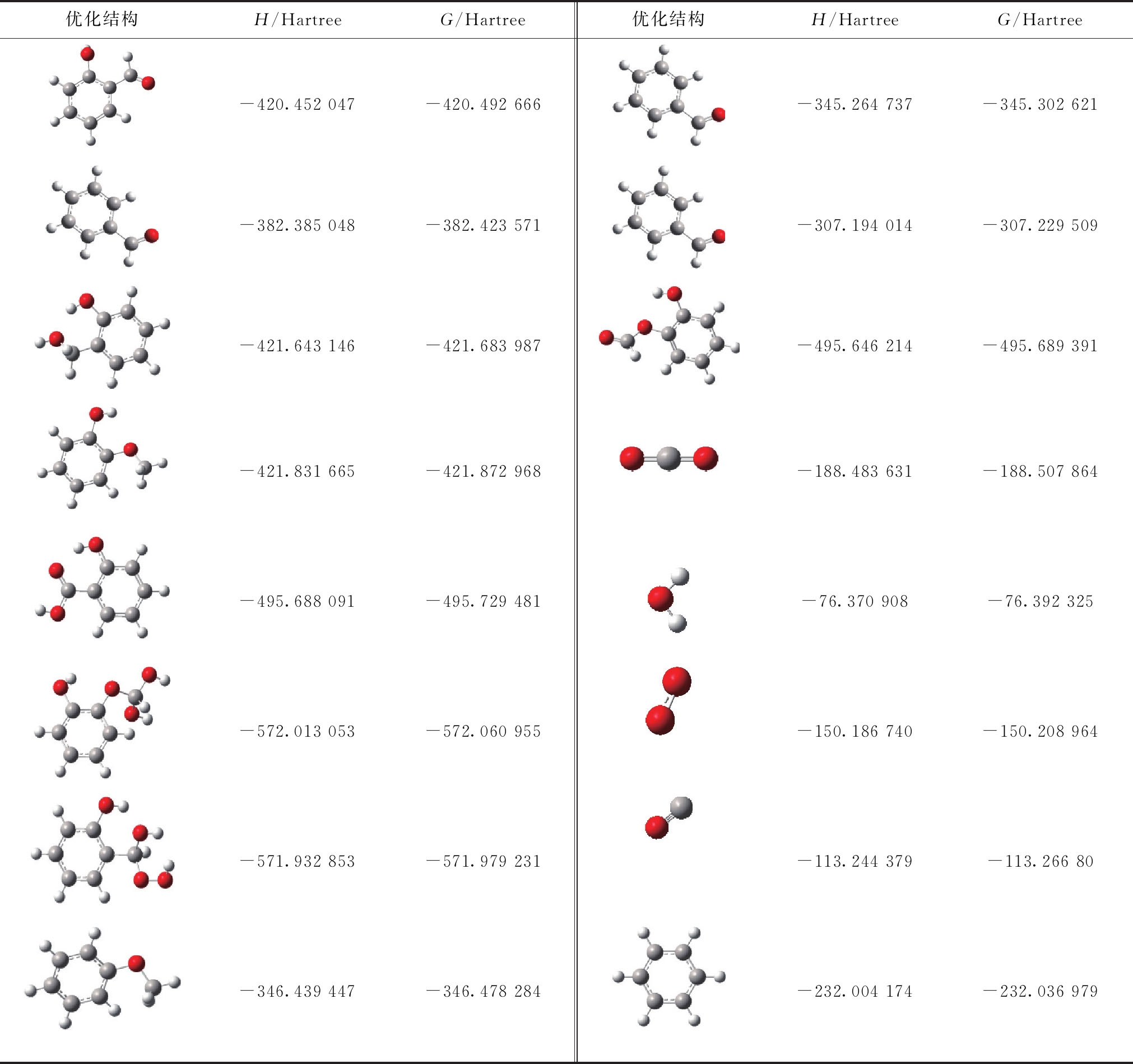
优化结构H/HartreeG/Hartree优化结构H/HartreeG/Hartree-420.452 047-420.492 666-345.264 737-345.302 621-382.385 048-382.423 571-307.194 014-307.229 509-421.643 146-421.683 987-495.646 214-495.689 391-421.831 665-421.872 968-188.483 631-188.507 864-495.688 091-495.729 481-76.370 908-76.392 325-572.013 053-572.060 955-150.186 740-150.208 964-571.932 853-571.979 231-113.244 379-113.266 80-346.439 447-346.478 284-232.004 174-232.036 979
注:![]() 表示氧原子;
表示氧原子;![]() 表示碳原子;
表示碳原子;![]() 表示氢原子;1 Hartree=2 625.5 kJ/mol。
表示氢原子;1 Hartree=2 625.5 kJ/mol。
表3 反应方程式的焓变(ΔH)吉布斯自由能变化值(ΔG)
Table 3 Changes of enthalpy and the Gibbs free energy
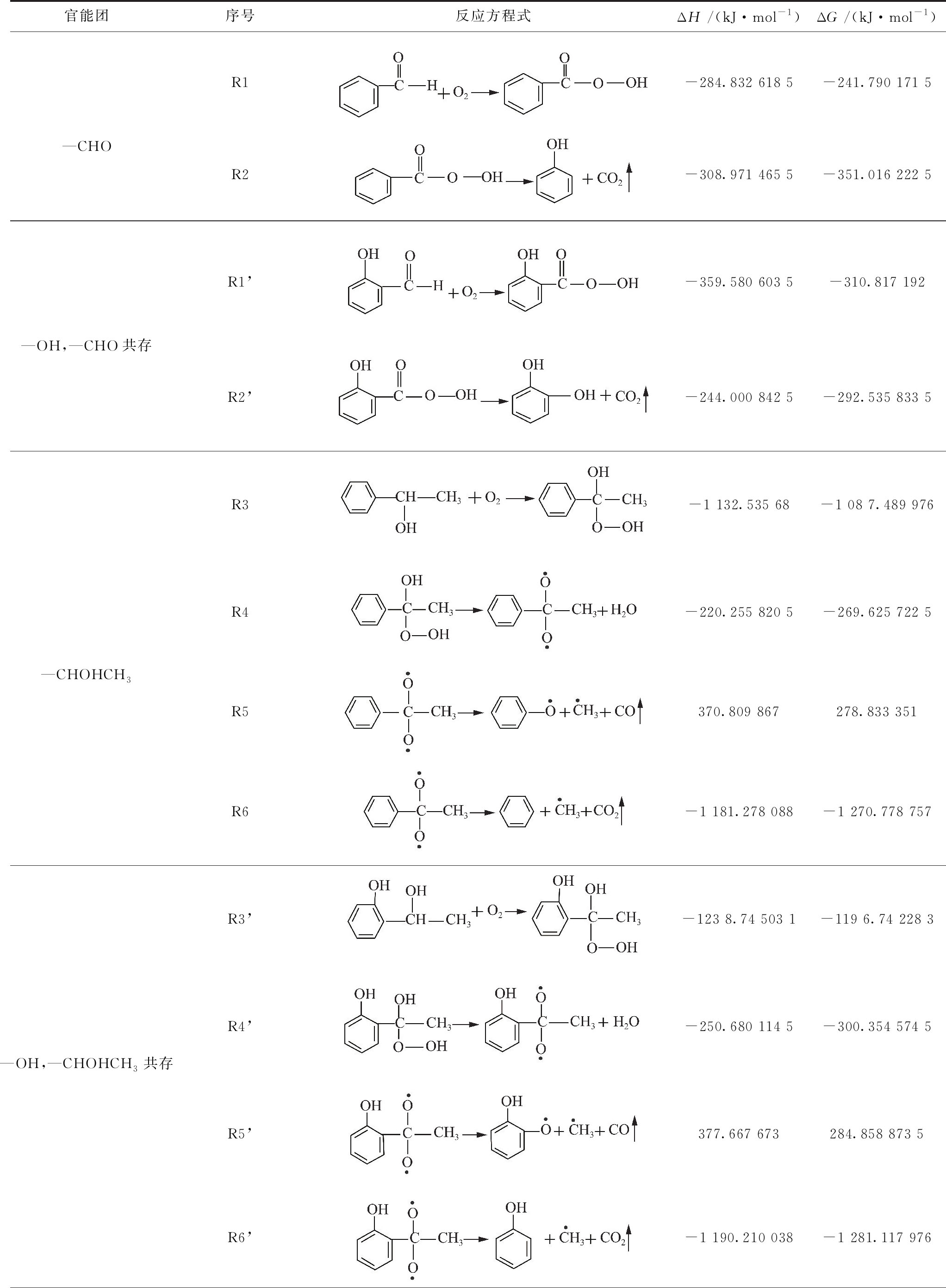
官能团序号反应方程式ΔH /(kJ·mol-1)ΔG /(kJ·mol-1)—CHOR1-284.832 618 5-241.790 171 5R2-308.971 465 5-351.016 222 5—OH,—CHO共存R1’-359.580 603 5-310.817 192R2’-244.000 842 5-292.535 833 5R3-1 132.535 68-1 08 7.489 976—CHOHCH3R4-220.255 820 5-269.625 722 5R5370.809 867278.833 351R6-1 181.278 088-1 270.778 757R3’-123 8.74 503 1-119 6.74 228 3—OH,—CHOHCH3共存R4’-250.680 114 5-300.354 574 5R5’377.667 673284.858 873 5R6’-1 190.210 038-1 281.117 976
续 表
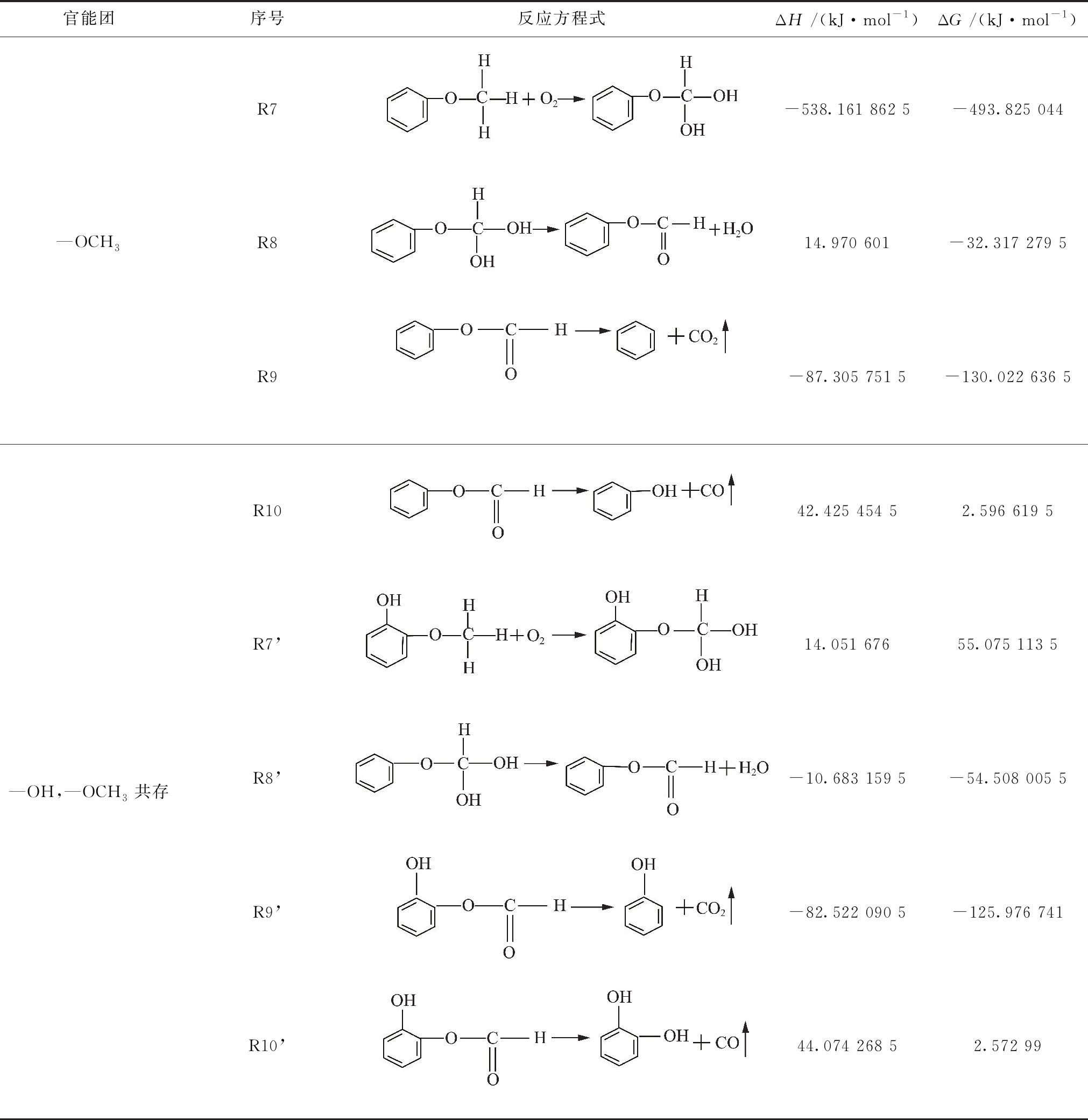
官能团序号反应方程式ΔH /(kJ·mol-1)ΔG /(kJ·mol-1)R7-538.161 862 5-493.825 044—OCH3R814.970 601-32.317 279 5R9-87.305 751 5-130.022 636 5R1042.425 454 52.596 619 5R7’14.051 67655.075 113 5—OH,—OCH3共存R8’-10.683 159 5-54.508 005 5R9’-82.522 090 5-125.976 741R10’44.074 268 52.572 99
R2,R6和R9与R5和R10分别表示煤自燃指标气体的生成过程,其中R2,R6和R9为CO2的生成反应,R6和R10表示CO的产生过程。表3中的数据显示R2,R6,和R9的焓变(ΔH)和吉布斯自由能变化值(ΔG)均小于零,表明煤自燃过程中CO2气体的生成是一个自发的放热反应,而R5和R10的吉布斯自由能变化值(ΔG)和焓变(ΔH)皆大于零,说明CO气体的生成为非自发吸热反应,这也就解释了为何在程序升温中一开始就有CO2产生,而只有当煤的温度升至60~80 ℃时才会有CO析出[32-33]。对比分析R1~R10与R1’~R10’的吉布斯自由能变化值(ΔG)和焓变(ΔH)发现 —OH对侧链基团吸附氧气后生成的过氧化氢物的分解反应无明显影响。
3 结 论
(1)侧链活性基团 —CHO,—CHOHCH3和—OCH3中氧原子附近呈负电势,为亲电反应活性位点,氢原子附近为呈正电势,为亲核反应活性位点。
(2)侧链活性基团的反应活性为 —CHO>—OCH3 >—CHOHCH3,其LUMO的成键能力为—CHOHCH3>—OCH3 >—CHO。侧链活性基团与氧气复合的难易程度主要由他们LUMO的成键能力决定,成键能力越强,复合反应越容易发生。
(3)—OH可以改变侧链活性基团的前线轨道特性,因而对侧链活性基团与氧气的复合反应过程有显著影响,而对复合反应产物—过氧化氢物的分解反应无明显影响。
(4)由于 —OH提高了 —CHO的亲核反应能力和 —CHOHCH3的LUMO成键能力,故当 —OH处于邻位时,—CHO和 —CHOHCH3都更容易与氧气发生复合反应。然而,当 —OH与—OCH3共存时,—OCH3的亲核反应活性位点消失,故其与氧气的复合反应从原来的自发放热反应转变为非自发的吸热反应。
(5)煤自燃过程中生成CO2的生成是一个自发式的放热反应,而CO的生成则为非自发的吸热反应。
[1] 国家安全生产监督管理总局,国家煤矿安全生产监察局.煤矿安全技术专家会诊资料汇编[M].北京:国家煤矿安全生产监察局,2019,206,209,691-192.
[2] FIRAT A,ERHAN T A.Coal resource estimation using Gaussian copula[J].International Journal of Coal Geology,2017,175(15):1-9.
[3] 徐精彩.煤自燃危险区域判定理论[M].北京:煤炭工业出版社,2001:25-29.
[4] 位爱竹.煤炭自燃自由基反应机理的实验研究[D].徐州:中国矿业大学,2008:32-38.
WEI Aizhu.Experimental study on free radical reaction mechanism of coal spontaneous combustion[D].Xuzhou:China University of Mining and Technology,2008:32-38.
[5] WANG H,DLUGOGORSKI B Z,KENNEDY E M.Kinetic modeling of low-temperature oxidation of coal[J].Combustion and Flame,2002,131(4):452-469.
[6] LYNCH B M,LANCASTER L,ANTHONY M J,Carbonyl groups from chemically and thermally promoted decomposition of peroxides on coal surfaces:Detection of specific types using photoacoustic infrared fourier transform spectroscopy[J].Fuel,2987,66:979-983.
[7] 王继仁,金智新,邓存宝.煤自燃量子化学理论[M].北京:科学出版社,2007:195-207.
[8] 邓存宝.煤的自燃机理及自燃性危险指数研究[D].葫芦岛:辽宁工程技术大学,2006:12-35.
DENG Cunbao.Study on the mechanism of spontaneous combustion and the hazard index of spontaneous combustion of coal[D].Huludao:Liaoning Technical University,2006:12-35.
[9] LI Kejiang,RITA Khanna,ZHANG Jianliang,et.al.Comprehensive investigation of various structural features of bituminous coals using advanced analytical techniques[J].Energy & Fuels.2015,29:7187-7189.
[10] NDAJI F E,BUTTERFIELD I M,MARK T K.Changes in the macromolecular structure of coals with pyrolysis temperature[J].Fuel,1997,76(2):169-177.
[11] 王彩萍,邓军,王凯.不同煤阶煤氧化过程中活性基团的红外光谱特征研究[J].西安科技大学学报,2016,36(3):320-323.
WANG Caiping,DENG Jun,WANG Kai.Infrared spectrum charateristics of active groups during oxidation process for different ranks of coal[J].Journal of Xi’an University of Science and Technology,2016,36(3):320-323.
[12] XU Qin,YANG Shengqiang,HU Xincheng,et al.Low-temperature oxidation of free radicals and functional groups in coal during the extraction of coalbed methane[J].Fuel,2019,239:429-436.
[13] 杨漪.基于氧化特性的煤自燃阻化剂机理及性能研究[D].西安:西安科技大学,2015:55-75.
YANG Yi.Research on mechanism and performance of retarder based on oxidation characteristics of spontaneous combustion of coal[D].Xi’an:Xi’an University of Science and Technology,2015:55-75.
[14] ZHANG Yutao,YANG Chaoping,LI Yaqing,et al.Ultrasonic extraction and oxidation characteristics of functional groups during coal spontaneous combustion[J].Fuel,2019,242:287-294.
[15] 王德明,辛海会,戚绪尧,等.煤自燃中的各种基元反应及相互关系:煤氧化动力学理论及应用[J].煤炭学报,2014,39(8):1667-1673.
WANG Deming,XIN Haihui,QI Xuyao,et al.Mechanism and relationships of elementary reactions in spontaneous combustion of coal:The coal oxidation kinetics theory and application[J].Journal of China Coal Society,2014,39(8):1667-1673.
[16] 葛岭梅,薛韩玲,徐精彩,等.对煤分子中活性基团氧化机理的分析[J].煤炭转化,2001,24(3):23-28.
GE Lingmei,XUE Hanling,XU Jingcai,et al.Study on the oxidation mechanism of active groups of coal[J].Coal Conversion,2001,24(3):23-28.
[17] 张嬿妮.煤氧化自燃微观特征及其宏观表征研究[D].西安:西安科技大学,2012:68-74.
ZHANG Yanni.Study on the microcosmic characteristics and macro parameters in the process of coal oxidation and spontaneous combustion[D].Xi’an:Xi’an University of Science and Technology,2012:68-74.
[18] SHI Ting,WANG Xiaofang,DENG Jun,et al.The mechanism at the initial stage of the room-temperature oxidation of coal[J].Combustion and Flame,2005,140(4):332-345.
[19] XU Tao.Heat effect of the oxygen-containing functional groups in coal during spontaneous combustion processes[J].Advanced Power Technology,2017,28:1841-1848.
[20] RIESSER B,STARSINIC M,SQUIRES E,et al.Determination of aromatic and aliphatic CH groups in coal by FT-I.R.:2.Studies of coals and vitrinite concentrates[J].Fuel,1984,63(9):1253-1261.
[21] SOLOMON P R,ROBERT M.CARANGELO.FT-I.R.analysis of coal:2.Aliphatic and aromatic hydrogen concentration[J].Fuel,1988,67(7):949-959.
[22] WANG Jing,HAN Yuzhen,CHEN Bozhen,et al.Mechanisms of methane generation from anthracite at low temperatures:Insights from quantum chemistry calculations[J].Science Direct,2017,42:18922-18929.
[23] 葛岭梅,李建伟.神府煤低温氧化过程中官能团结构演变[J].西安科技学院报,2003,23(2):187-190.
GE Lingmei,LI Jianwei.Evolution of functional groups in low-temperature oxidized Shenfu coal[J].Journal of Xi’an University of Science and Technology,2003,23(2):187-190.
[24] 唐一博.基于模型化合物的煤表面活性基团低温氧化研究[D].徐州:中国矿业大学,2014:32-46.
TANG Yibo.Low-temperature oxidation of coal-surface-groups based on model compounds[D].Xuzhou:China University of Mining and Technology,2014:32-46.
[25] LIN S K.Advanced organic chemistry.Part A:Structure and mechanism.Fourth Edition.By Francis A.Carey[J].Molecules,2000,5(12):1528-1629.
[26] LI Xiaodong,TANG Yongjian,WANG Zhaoyang.A DFT investigation on hydrogen adsorption based on Alkali-metal organic complexes[J].Chinese Journal of Structural Chemistry,2010,29(9):1404-1410.
[27] 席婵娟,邓耿.物理有机化学:结构与原理[M].北京:高等教育出版社,2017:265-280.
[28] 王怀亮.共轭效应与反应活性[J].山西师大学报(自然科学版),1994,8(2):40-43.
WANG Huailiang.Effect of conjugation and reactivity[J].Journal of Shanxi Teacher’s University (Natural Science Edition),1994,8(2):40-43.
[29] ZHANG Yutao,LI Yaqing,HUANG Yao,et al.Characteristics of mass,heat and gaseous products during coal spontaneous combustion using TG/DSC-FTIR technology[J].Journal of Thermal Calorimetry,2018,131:2963-2974.
[30] ZHANG Yutao,LIU Yurui,SHI Xueqiang,et al.Risk evaluation of coal spontaneous combustion on the basis of auto-ignition temperature[J].Fuel,2018,233:68-76.
[31] ZHANG Yutao,SHI Xueqiang,LI Yaqing,et al.Characteristics of carbon monoxide production and oxidation kinetics during the decaying process of coal spontaneous combustion[J].The Canadian Journal of Chemical Engineering,2017,96(8):1752-1761.
[32] 赵婧煜.淮南煤氧化动力学过程及其微观结构演化特征研究[D].西安:西安科技大学,2017:43-46.
ZHAO Jingyu.Study on the kinetics and micro-structures characteristics of Huainan coal in the oxidation process[D].Xi’an:Xi’an University of Science and Technology,2017:43-46.
[33] 周东,刘贞堂,钱继发,等.采空区内煤自燃气体特征及产生规律分析[J].工矿自动化,2019,45(3):18-22.
ZHOU Dong,LIU Zhentang,QIAN Jifa,et al.Analysis of gas characteristics and generation rules of coal spontaneous combustion in goaf[J].Industry and Mine Automation,2019,45(3):18-22.
